题目内容
3.下列反应的离子方程式书写不正确的是( )| A. | 向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全:Ba2++2OH-+H++SO42-+NH4+═BaSO4↓+NH3•H2O+H2O | |
| B. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O | |
| C. | 硫化钠的水解:S2-+H2O═HS-+OH- | |
| D. | NaHCO3溶液中滴加少量澄清石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- |
分析 A.至刚好沉淀完全,以1:1反应生成硫酸钡、水、一水合氨;
B.发生氧化还原反应生成碘化亚铁、碘、水;
C.水解分步进行,以第一步为主,水解生成硫氢根离子和氢氧根离子;
D.少量澄清石灰水完全反应,生成碳酸钙、碳酸钠和水.
解答 解:A.向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全的离子反应为Ba2++2OH-+H++SO42-+NH4+═BaSO4↓+NH3•H2O+H2O,故A正确;
B.Fe(OH)3溶于氢碘酸的离子反应为2I-+2Fe(OH)3+6H+═2Fe2++6H2O+I2,故B错误;
C.硫化钠的水解的离子反应为S2-+H2O═HS-+OH-,故C正确;
D.NaHCO3溶液中滴加少量澄清石灰水的离子反应为2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32-,故D正确;
故选B.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重与量有关的离子反应、氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
相关题目
13.只用胶头滴管和试管通过两试剂的互滴,能区别的下列溶液( )
| A. | NaAlO2和Al2(SO4)3 | B. | NaHCO3和Ca(OH)2 | C. | AlCl3和氨水 | D. | HCl和Na2CO3 |
14.下列实验操作符合安全要求的是( )
| A. | 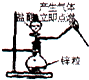 | B. |  | C. |  | D. |  |
18.下列说法不正确是( )
| A. | 用量筒量取一定量液体时,先从试剂瓶中直接倒入大部分试剂于量筒中,至接近刻度时改用胶头滴管,逐滴加入至刻度 | |
| B. | 实验室制氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液 | |
| C. | N2O5在四氯化碳溶液中分解为NO2和O2,可用分光光度计测定其化学反应速率 | |
| D. | 物质的分离提纯方法之一为“筛分:如胶体--半透膜法分离提纯;悬浊液--过滤分离,本质上就是依据所分离粒子的直径大小选择具有合适孔径的筛子 |
8.某溶液中含有NH4+、Fe2+、Fe3+、Al3+四种离子,若向溶液中先滴加过量的NaOH溶液,然后再滴加过量的稀盐酸,则溶液中离子数目保持不变的是( )
| A. | Al3+ | B. | NH4+ | C. | Fe3+ | D. | Fe2+ |
15.下列说法中不正确的是( )
| A. | 在燃煤中加入石灰石可减少SO2排放,发生的反应为2CaCO3+2SO2+O22CO2+2CaSO4 | |
| B. | CO2通入水玻璃可以得到硅酸沉淀 Na2SiO3+CO2+H2O═Na2CO3+H2SiO3↓ | |
| C. | 硅主要以单质、氧化物、硅酸盐的形式存在于自然界中 | |
| D. | 氢氟酸能够雕刻玻璃,故不能用玻璃瓶在盛装氢氟酸 SiO2+4HF═SiF4↑+2H2O |
 )4种有机物分别在一定条件下与H2充分反应.
)4种有机物分别在一定条件下与H2充分反应.