题目内容
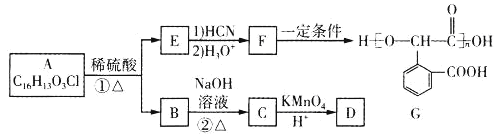
【题目】根据下面的反应路线及所给信息填空:
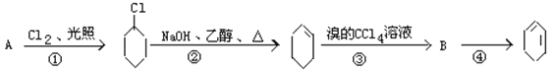
(1)A的结构简式是_____________,名称是_______________________;
(2)①的反应类型______________,②的反应类型__________________;
(3)反应②的化学方程式_______________________________;
反应④的化学方程式______________________________。
【答案】![]() 环己烷取代反应消去反应
环己烷取代反应消去反应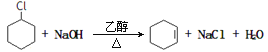
![]() +2NaOH
+2NaOH![]()
![]() +2NaBr+2H2O
+2NaBr+2H2O
【解析】
由合成路线可知,反应①为光照条件下的取代反应,所以A为![]() ,反应②为卤代烃发生的消去反应,反应③为环己烯的加成反应,则B为
,反应②为卤代烃发生的消去反应,反应③为环己烯的加成反应,则B为![]() ,反应④为卤代烃的消去反应,生成环己二烯,结合物质的性质及化学用语来解答。
,反应④为卤代烃的消去反应,生成环己二烯,结合物质的性质及化学用语来解答。
(1)由上述分析可知,A为![]() ,为环己烷,故答案为:
,为环己烷,故答案为:![]() ;环己烷;
;环己烷;
(2)反应①为取代反应,②为消去反应,故答案为:取代反应;消去反应;
(3)反应②是一氯环己烷发生卤代烃的消去反应生成环己烯,反应化学方程式为: ,反应④是卤代烃在氢氧化钠醇溶液、加热条件下发生的消去反应,反应方程式为:
,反应④是卤代烃在氢氧化钠醇溶液、加热条件下发生的消去反应,反应方程式为:![]() +2NaOH
+2NaOH![]()
![]() +2NaBr+2H2O,故答案为:
+2NaBr+2H2O,故答案为: ;
;![]() +2NaOH
+2NaOH![]()
![]() +2NaBr+2H2O。
+2NaBr+2H2O。

 阅读快车系列答案
阅读快车系列答案【题目】汽车尾气中的主要污染物为NOx、CO等有害物质。目前,已研究出了多种消除汽车尾气污染的方法。
I.催化剂存在时用H2将NO还原为N2。
已知: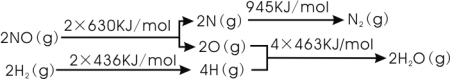
则H2还原NO生成氮气和水蒸气的热化学方程式是:______________________________。
II.用活性炭还原处理氮氧化物,有关反应为C(s)+2NO(g)![]() N2(g)+CO2(g)△H=QkJ/mol,在2L恒容密闭器中加入足量的C与NO反应,所得实验数据如表
N2(g)+CO2(g)△H=QkJ/mol,在2L恒容密闭器中加入足量的C与NO反应,所得实验数据如表
实验编号 | 温度/℃ | 起始时NO的物质的量/mol | 平衡时N2的物质的量/mol |
1 | 700 | 0.40 | 0.09 |
2 | 800 | 0.24 | 0.08 |
(1)写出该反应的平衡常数表达式________________________________________。
(2)结合表中数据,判断该反应的Q___0(填“>”或“<”),理由是________________________。.
(3)用电子式表示产物CO2的形成过程_________________________________________。
(4)判断该反应达到平衡的依据是____________
a.若容器内气体密度恒定,反应达到平衡状态
b.若容器内各气体浓度恒定,反应达到平衡状态
c.若容器内压强恒定,反应达到平衡状态
d.若2υ正(NO)=υ逆(N2),反应达到平衡状态