题目内容
【题目】绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。
回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,滴加___溶液,溶液颜色无明显变化,由此可知样品中无Fe3+。
(2)为测定绿矾中结晶水含量,称石英玻璃管(带开关K1和K2)(设为装置A)的质量,记为m1g。将样品装入石英玻璃管中,再次称其质量,记为m2g。按如图连接好装置进行实验。
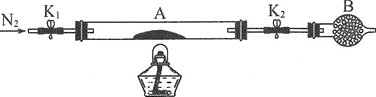
①仪器B的名称是___。
②将下列实验操作步骤正确排序___(填字母);重复上述操作步骤,直至A质量不变,记为m3g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2 d.打开K1和K2,缓缓通入N2 e.称量A f.冷却至室温
③根据实验记录,计算绿矾化学式,结晶水数目x=___。若实验时按a、d次序操作,则使x___(填偏大偏小或无影响)。
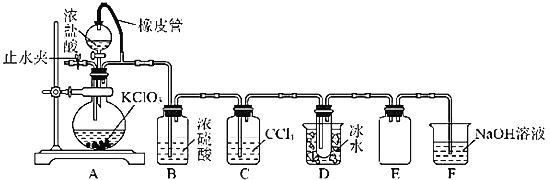
(3)为探究硫酸亚铁的分解产物,将(2)中已质量不变的装置A接入如图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。

①C、D中的溶液依次为___(填字母),可观察到C、D中有气泡冒出。
a.品红 b.NaOH C.BaCl2 d.Ba(NO3 )2 e.浓硫酸
②写出硫酸亚铁高温分解反应的化学方程式:___。
【答案】KSCN (球形)干燥管 dabfce ![]() 偏小 c、a 2FeSO4
偏小 c、a 2FeSO4![]() Fe2O3+SO2↑+SO3↑
Fe2O3+SO2↑+SO3↑
【解析】
(1)绿矾是FeSO4·7H2O,Fe2+与SCN-混合不显血红色,Fe3+与SCN-混合出现血红色,据此分析;
(2)①根据仪器的特点判断仪器的名称;
②实验时,为避免Fe2+被氧化,应先通入氮气,冷却水注意关闭开关,防止氧气的进入;
③加热绿矾,绿矾失去结晶水,即结晶水的质量为(m2-m3)g,FeSO4的质量为(m3-m1)g,a、d次序操作,造成FeSO4被氧化,据此分析;
(3)FeSO4高温分解可生成Fe2O3、SO2、SO3,C为BaCl2溶液,用于检验SO3,D为品红,用于检验SO2,据此分析。
(1)在试管中加入少量绿矾样品,加水溶解。滴加KSCN溶液,溶液颜色无明显变化,说明溶液中不存在铁离子;
(2)![]() 据图所示可知,仪器B的名称是:球形干燥管;
据图所示可知,仪器B的名称是:球形干燥管;
![]() 将下列实验操作步骤正确排序:打开
将下列实验操作步骤正确排序:打开![]() 和
和![]() ,缓缓通入
,缓缓通入![]() 以赶尽装置中的空气;点燃酒精灯,加热使绿矾失去结晶水;熄灭酒精灯停止实验;冷却至室温;关闭
以赶尽装置中的空气;点燃酒精灯,加热使绿矾失去结晶水;熄灭酒精灯停止实验;冷却至室温;关闭![]() 和
和![]() 防止水蒸气进入装置A内;称量A;故实验操作步骤正确排序为:dabfce;
防止水蒸气进入装置A内;称量A;故实验操作步骤正确排序为:dabfce;
![]() 根据实验记录,
根据实验记录,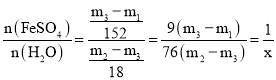 ,绿矾化学式中结晶水数目
,绿矾化学式中结晶水数目![]() ,若实验时按先点燃酒精灯加热,再打开
,若实验时按先点燃酒精灯加热,再打开![]() 和
和![]() ,则A中固体会与空气先反应,加热过程中硫酸亚铁被空气氧化为硫酸铁,导致
,则A中固体会与空气先反应,加热过程中硫酸亚铁被空气氧化为硫酸铁,导致![]() 增大,使x偏小;
增大,使x偏小;
(3)![]() 受热分解可产生二氧化硫或三氧化硫,实验C中的溶液氯化钡检验吸收是否有三氧化硫,不能用硝酸钡,因为能将二氧化硫氧化、D中的溶液为品红用来检验二氧化硫的存在;
受热分解可产生二氧化硫或三氧化硫,实验C中的溶液氯化钡检验吸收是否有三氧化硫,不能用硝酸钡,因为能将二氧化硫氧化、D中的溶液为品红用来检验二氧化硫的存在;
![]() 因为D中所盛的试剂为品红溶液,观察到溶液褪色,则说明产物中有二氧化硫和三氧化硫,根据氧化还原反应的原理,则生成物有氧化铁,所以硫酸亚铁高温分解反应的化学方程式:
因为D中所盛的试剂为品红溶液,观察到溶液褪色,则说明产物中有二氧化硫和三氧化硫,根据氧化还原反应的原理,则生成物有氧化铁,所以硫酸亚铁高温分解反应的化学方程式:![]() 。
。

【题目】用沉淀滴定法快速测定待测溶液中c(Cl-)。
滴定的主要步骤:
a.取待测溶液25.00mL于锥形瓶中。
b.加入25.00mL 0.1000mol·L-1 AgNO3溶液(过量),使Cl-完全转化为AgCl沉淀。
c.加入少量硝基苯并振荡,使其覆盖沉淀,避免沉淀与溶液接触。
d.加入NH4Fe(SO4)2溶液作指示剂。
e.用0.1000mol·L-1NH4SCN溶液滴定过量的Ag+,使其恰好完全转化为AgSCN沉淀。
f.重复上述操作两次。
三次测定数据如下表:
实验序号 | 1 | 2 | 3 |
消耗NH4SCN标准溶液体积/mL | 10.24 | 10.02 | 9.98 |
g.数据处理。
已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12。
(1)滴定终点的现象为______________________________。
(2)步骤c中加入硝基苯的目的是______________________________。
(3)计算待测溶液中c(Cl-)=__________mol·L-1。
(4)判断下列操作对c(Cl-)测定结果的影响(填“偏高”、“偏低”或“无影响”)
①若在配制AgNO3标准溶液时,烧杯中的溶液有少量溅出,则测定结果__________;
②若在滴定终点读取滴定管刻度时,仰视标准液液面,则测定结果__________。
【题目】一定条件下,两体积均为1 L的容器中发生反应:CO(g)+2H2(g) ![]() CH3OH(g) ΔH。容器中起始各物质的物质的量如下表所示,两容器中c(H2)随时间t的变化如下图所示。
CH3OH(g) ΔH。容器中起始各物质的物质的量如下表所示,两容器中c(H2)随时间t的变化如下图所示。
容器 | 温度 | CO | H2 | CH3OH |
Ⅰ | T1℃ | a mol | 2 mol | 0 mol |
Ⅱ | T1℃ | 0.5 mol | 1 mol | 0 mol |

下列说法正确的是
A.0~5 min时,容器Ⅰ中v(CO)=0.1 mol·L-1·min-1
B.a>1
C.若容器Ⅱ温度改变为T2(T2>T1)时,平衡常数K=1,则ΔH<0
D.T1℃时,若向容器Ⅰ中充入CO、H2、CH3OH各1 mol,反应将向逆反应方向进行
【题目】(1)将Cl2通入水中,Cl2部分与水反应:Cl2+H2![]() OH++Cl-+HClO。若要减少Cl2的溶解,可在氯水中加入少量___。
OH++Cl-+HClO。若要减少Cl2的溶解,可在氯水中加入少量___。
A.AgNO3晶体 B.CaCO3粉末 C.NaCl晶体 D.蒸馏水 E.浓盐酸
(2)在一定条件下,同时加入CO、H2O(g)、CO2、H2于一密闭容器中发生如下反应:CO+H2O(g)![]() CO2+H2,反应开始时向右进行。下列说法中不正确的是___。
CO2+H2,反应开始时向右进行。下列说法中不正确的是___。
A.反应开始时,正反应速率大于逆反应速率
B.反应开始时,正反应速率最大,逆反应速率为零
C.随着反应的进行,正反应速率逐渐减小,最后为零
D.随着反应的进行,逆反应速率增大,正反应速率减小,最后相等
(3)一定条件下(温度恒定),SO2与O2反应的浓度随时间的变化如下表。
时间/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
c(SO2)/(mol·L-1) | 1.0 | |||||||
c(O2)/(mol·L-1) | 0.5 | 0.35 | 0.25 | 0.18 | 0.1 | 0.05 | 0.05 | 0.05 |
c(SO3)/(mol·L-1) | 0 | 0.3 | 0.5 | 0.65 | 0.8 | 0.9 | 0.9 | 0.9 |
由上表数据计算:
A.30~40min时间段,以SO2表示的反应速率为___;
B.该温度下,正反应的平衡常数的值为___;
C.平衡时,SO2的转化率为___。
(4)电解尿素的碱性溶液制氢气的装置示意图见如图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为___。

(5)3.04g铜镁合金完全溶解于100mL密度为1.40g·cm-3、质量分数为63%的硝酸中,得到NO2气体2688mL(标准状况),向反应后的溶液中加入1.0mol·L-1NaOH溶液,当金属离子全部沉淀时,得到5.08g沉淀。则加入NaOH溶液的体积是___mL。