题目内容
下列各组气体在常温下能共存且能用向上排空气法收集的是
| A.NO和O2 | B.HCl和NH3 | C.H2和CO | D.SO2和CO2 |
D
解析试题分析:NO和氧气极易化合生成NO2,氯化氢和氨气极易化合生成氯化铵,均并能共存;氢气的密度小于空气的,应该用向下排空气法收集。CO的密度略小于空气的,且CO有毒,不能用向上排空气法收集,C不正确;D中的气体可以共存,且密度均大于空气的,可以用向上排空气法收集,答案选D。
考点:考查气体的性质和气体收集方法的判断
点评:常见气体的收集方法是:1.排水法,适用于不易溶于水的气体。例如氢气,氧气;2.向上排空气法,适用于比空气密度大,溶于水的气体,例如二氧化碳,氯气;3,向下排空气法,适用于比空气密度小,溶于水的气体,例如氨气。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
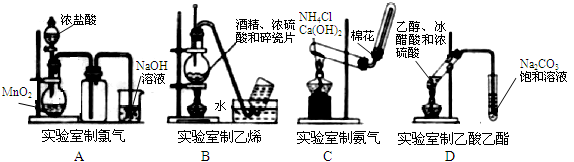
下列有关实验装置进行的相应实验,能达到实验目的的是
| A.用图1装置制取并收集干燥纯净的NH3 |
| B.用图2装置实验室制备Fe(OH)2 |
| C.装置3收集并测量Cu与浓硝酸反应产生的气体及体积 |
| D.装置4可用于实验室制取乙酸乙酯 |
下列实验不能达到预期目的的是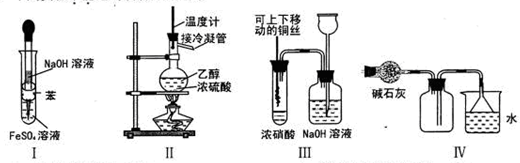
| A.利用I制取Fe(OH)2 | B.利用II装置制取CH2=CH2 |
| C.利用III装置进行铜与浓硝酸反应的实验 | D.利用IV装置收集NH3 |
下列实验设计或实验操作中,正确的是
| A.铜与浓硝酸反应制NO2:可采用下图装置 |
| B.分离乙酸和乙醇溶液:用分液漏斗进行分离 |
| C.稀硫酸和锌粒反应制取氢气:加入少许硫酸铜以加快反应速率 |
| D.鉴别Na2CO3溶液和NaHCO3溶液:分别向两种溶液滴加澄清石灰水至过量 |
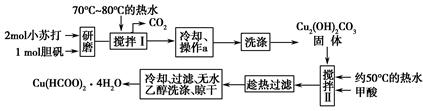
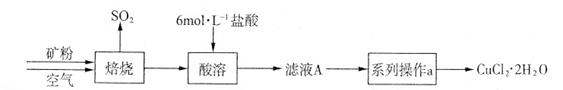
锌钡白是一种白色颜料。工业上是由ZnSO4与BaS溶液混合而成:BaS+ZnSO4=ZnS↓+BaSO4↓。请根据以下工业生产流程回答有关问题。
I.ZnSO4溶液的制备与提纯:
有关资料:a.菱锌矿的主要成分是ZnCO3,含少量SiO2、FeCO3、Cu2(OH)2CO3等;b.Zn(OH)2与Al(OH)3相似,能溶于过量的NaOH溶液生成Na2ZnO2;
(1)滤渣1的化学式为 ;②中使用的氧化剂最好是下列的 (填序号)。
| A.Cl2 | B.H2O2 | C.KMnO4 | D.浓HNO3 |
(3)步骤④发生的离子反应方程式为 。
II.BaS溶液的制备

有关数据:Ba(s)+S(s)+2O2(g)=BaSO4(s) △H1 = -1473.2 kJ?mol-1
C(s)+ 1/2O2(g)=CO(g) △H2 = -110.5 kJ?mol-1
Ba(s)+ S(s)=BaS(s) △H3 = -460 kJ?mol-1
(4)若煅烧还原的产物仅为BaS和CO,则其反应的热化学方程式为:
。
Ⅲ.制取锌钡白
(5)如果Ⅰ中步骤⑤使用硫酸过量,产生的后果是 。


 CuCl42-(黄色)+4H2O。
CuCl42-(黄色)+4H2O。

