题目内容
向某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应A(g)+xB(g) 2C(g),达到平衡后,只改变反应的一个条件,测得容器中各物质的浓度、反应速率随时间变化的关系如图所示。下列说法正确的是
2C(g),达到平衡后,只改变反应的一个条件,测得容器中各物质的浓度、反应速率随时间变化的关系如图所示。下列说法正确的是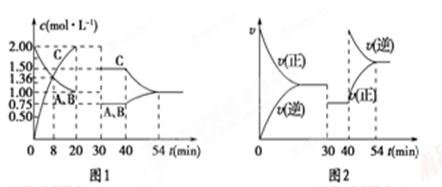
| A.30 min时改变的条件是降低温度,40 min时改变的条件是升高温度 |
| B.8 min前A的平均反应速率为0.08 mol/(L·min) |
| C.反应的化学方程式中的x=1,且正反应为吸热反应 |
| D.20 min后该反应的平衡常数均为4 |
B
解析图1可知该反应在20min时达到平衡,A和B减少的浓度相同,可以推断知x=1;由图2可知30min时,正、逆反应速率同时减少且相等,可以推断改变的条件是减少压强;40min时,正逆反应速率均增大且不相等,所以改变的条件是升高温度,且平衡向逆方向移动,正的是放热反应,A和C都错;由8min时A的转化率可以算出其平均速率为(2-1.36)÷8=0.08 mol/(L·min),B正确;根据图可求出20-40min内该反应的平衡常数K=4,40min时升高温度,平衡常数减少,D错。答案选B。

100 mL浓度为2 mol/L的盐酸跟过量的锌片反应,为减慢反应速率,又不影响生成氢气的总量,可采用的方法是
| A.加入适量NaCl溶液 | B.加入适量NaOH溶液 |
| C.加入数滴CuCl2溶液 | D.加入适量NaNO3溶液 |
可逆反应aA(g)+bB(g) cC(g)+dD(g)ΔH同时符合下列两图中各曲线的规律的( )
cC(g)+dD(g)ΔH同时符合下列两图中各曲线的规律的( )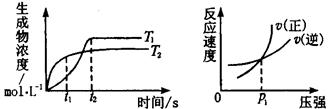
| A.a+b>c+d T1<T2 ΔH<0 |
| B.a+b>c+d T1<T2 ΔH>0 |
| C.a+b<c+d T1>T2 ΔH<0 |
| D.a+b>c+d T1>T2 ΔH>0 |
一定条件下,通过下列反应可以制备特种陶瓷的原料MgO,MgSO4(s) + CO(g)  MgO(s) + CO2(g) +SO2(g) △H>0该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
MgO(s) + CO2(g) +SO2(g) △H>0该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
| 选项 | x | y |
| A | 温度 | 容器内混合气体的密度 |
| B | CO的物质的量 | CO2与CO的物质的量之比 |
| C | SO2的浓度 | 平衡常数K |
| D | MgSO4的质量(忽略体积) | CO的转化率 |
一定条件下,将3molA和1molB两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g) 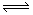 xC(g)+2D(s)。2min末该反应达到平衡,生成0.8molD,并测得C的浓度为0.2mol/L。下列判断正确的是( )
xC(g)+2D(s)。2min末该反应达到平衡,生成0.8molD,并测得C的浓度为0.2mol/L。下列判断正确的是( )
| A.该条件下此反应的化学平衡常数约为0.91 |
| B.A的平均反应速率为0.3mol/(L·s) |
| C.B的转化率为60% |
| D.若混合气体的密度不再改变时,该反应不一定达到平衡状态 |
某温度下,向2 L恒容密闭容器中充入1.0 mol A和1.0 mol B,反应A(g)+B(g)  C(g),经过一段时间后达到平衡。反应过程中测定的部分数据如表,下列说法正确的是
C(g),经过一段时间后达到平衡。反应过程中测定的部分数据如表,下列说法正确的是
| t/s | 0 | 5 | 15 | 25 | 35 |
| n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
A.反应在前5 s的平均速率v(A)=0.17 mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时c(A)=0.41 mol·L-1,则反应的ΔH>0
C.相同温度下,起始时向容器中充入2.0 mol C,达到平衡时,C的转化率大于80%
D.相同温度下,起始时向容器中充入0.20 mol A、0.20 mol B和1.0 mol C,反应达到平衡前v(正)<v(逆)
碘单质难溶于水却易溶于KI溶液。碘水中加入KI溶液发生反应:I2(aq)+I-(aq)  I(aq),该反应的平衡常数与温度的关系如图,下列说法不正确的是( )
I(aq),该反应的平衡常数与温度的关系如图,下列说法不正确的是( )
| A.上述正反应为放热反应 |
| B.上述体系中加入苯,平衡不移动 |
| C.可运用该反应原理除去硫粉中少量的碘单质 |
| D.实验室配制碘水时,为增大碘单质的溶解度可加入适量KI溶液 |
 2C(g)+2D(g) 在4种不同情况下反应速率分别如下,其中反应速率v最大的是
2C(g)+2D(g) 在4种不同情况下反应速率分别如下,其中反应速率v最大的是 1/2N2(g)+CO2(g) ΔH=-373.4 kJ·mol-1
1/2N2(g)+CO2(g) ΔH=-373.4 kJ·mol-1