题目内容
12.下列6个转化,其中不能通过一步反应实现的是( )①SiO2→Na2SiO3
②Al(OH)3-→Al2O3
③SiO2→H2SiO3
④Al2O3-→Al(OH)3
⑤Na2O2→NaCl
⑥Al-→AlO2-.
| A. | ①② | B. | ③④ | C. | ②③ | D. | ⑤⑥ |
分析 ①二氧化硅和氢氧化钠溶液反应生成硅酸钠和水;
②氢氧化铝受热分解生成氧化铝;
③二氧化硅不能溶于水得到硅酸;
④氧化铝不能一步反应得到氢氧化铝;
⑤过氧化钠和盐酸反应生成氯化钠、水和氧气;
⑥铝和氢氧化钠溶液反应生成偏氯酸钠和氢气;
解答 解:①二氧化硅和氢氧化钠溶液反应生成硅酸钠和水,SiO2+2NaOH=Na2SiO3+H2O,一步反应实现,故①不符合;
②氢氧化铝受热分解生成氧化铝,2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O,一步反应实现,故②不符合;
③二氧化硅不能溶于水得到硅酸,一步反应不能实现,故③符合;
④氧化铝不能一步反应得到氢氧化铝,一步反应不能实现,故④符合;
⑤过氧化钠和盐酸反应生成氯化钠、水和氧气,2Na2O2+4HCl=4NaCl+2H2O+O2↑,一步反应实现,故⑤不符合;
⑥铝和氢氧化钠溶液反应生成偏氯酸钠和氢气,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,故⑥不符合;
故选B.
点评 本题考查了物质性质的理解应用,掌握物质性质和反应特征是关键,注意知识的积累,题目较简单.

练习册系列答案
相关题目
7.用单分子油膜法测出油酸分子(视为球形)的直径后,还要下列哪一个物理量就可以计算出阿伏加德罗常数( )
| A. | 油滴的体积 | B. | 油滴的质量 | C. | 1 mol油酸的体积 | D. | 油酸的摩尔质量 |
15.元素在元素周期表中的位置可以反映元素的原子结构和性质,下列说法正确的是( )
| A. | 同一元素不可能既表现金属性,又表现非金属性 | |
| B. | 第三周期元素的最高正化合价等于它所处的主族序数 | |
| C. | 短周期中同主族元素的最外层电子数及化学性质完全相同 | |
| D. | 同周期元素的原子半径从左到右依次减小 |
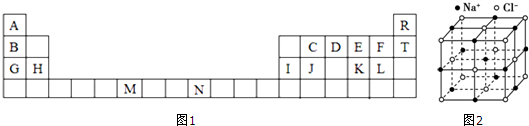
 .
.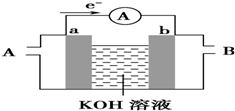 (1)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2FeO4+8H2O $?_{充电}^{放电}$3Zn(OH)2+2Fe(OH)3+4KOH. 请回答下列问题:
(1)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2FeO4+8H2O $?_{充电}^{放电}$3Zn(OH)2+2Fe(OH)3+4KOH. 请回答下列问题: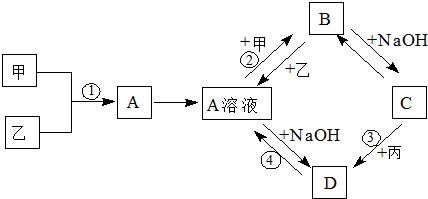
 .
.