题目内容
二氧化硫是一种大气污染物,研究对NO2、SO2、CO等大气污染气体的处理有重要意义,某化学实验爱好小组欲探究SO2的性质,设计如下方案:
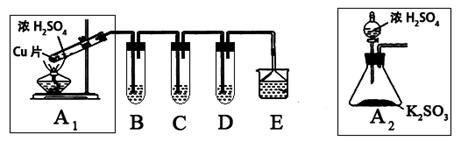
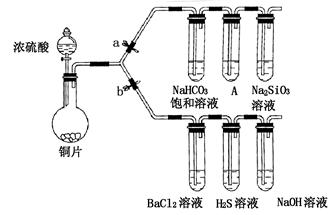
(1)B、C、D分别用于检验SO2的还原性、氧化性和漂白性。其中B、C分别为碘水和硫化氢的水溶液,则D中所盛试剂为_________,B中反应的离子方程式为:_________________。
(2)为了实现绿色实验的目标,某同学重新设计了如上右图A2的制取装置来代替A1装置,与A1装置相比,A2装置的优点是:________________________________(任写一点即可)。
(3)E中用氨水吸收尾气中的SO2,“吸收液”中可能含有OH-、SO32-、SO42-、HSO3-等阴离子。已知亚硫酸氢盐一般易溶于水,SO2也易溶于水。现有仪器和试剂为:小烧杯、试管、玻璃棒、胶头滴管、过滤装置和滤纸;2mol/L盐酸、1mol/L BaCl2溶液、1mol/L Ba(OH)2溶液、品红溶液、蒸馏水。
请设计实验证明“吸收液”中存在SO32-和HSO3-,完成下表的实验操作、预期现象和结论:

(1)B、C、D分别用于检验SO2的还原性、氧化性和漂白性。其中B、C分别为碘水和硫化氢的水溶液,则D中所盛试剂为_________,B中反应的离子方程式为:_________________。
(2)为了实现绿色实验的目标,某同学重新设计了如上右图A2的制取装置来代替A1装置,与A1装置相比,A2装置的优点是:________________________________(任写一点即可)。
(3)E中用氨水吸收尾气中的SO2,“吸收液”中可能含有OH-、SO32-、SO42-、HSO3-等阴离子。已知亚硫酸氢盐一般易溶于水,SO2也易溶于水。现有仪器和试剂为:小烧杯、试管、玻璃棒、胶头滴管、过滤装置和滤纸;2mol/L盐酸、1mol/L BaCl2溶液、1mol/L Ba(OH)2溶液、品红溶液、蒸馏水。
请设计实验证明“吸收液”中存在SO32-和HSO3-,完成下表的实验操作、预期现象和结论:
| 实验操作 | 预期现象与结论 |
| 步骤1:取适量“吸收液”于小烧杯中,用胶头滴管取1mol/L BaCl2溶液向小烧杯滴加直至过量。 | 若出现白色浑浊,则溶液中存在SO32-或 SO42-。 |
| 步骤2:将小烧杯中的浊液过滤、洗涤,再用适量水把附在滤纸上的固体冲入另一小烧杯中;向冲下的固体 ___________________________________________________ | _________________________ ______________________________________________ |
| 步骤3:_______ _______________________ ___________________________________________________ | _________________________ |
(1)品红溶液 (1分)
SO2 + I2 + 2H2O = SO42- +2I- + 4H+(2分,电荷不守恒0分;化学式任错一个0分)
(2)①不用加热,安全性能高。
②易于控制反应进行,反应更充分。(任写一个,合理答案均给1分)
(3)
SO2 + I2 + 2H2O = SO42- +2I- + 4H+(2分,电荷不守恒0分;化学式任错一个0分)
(2)①不用加热,安全性能高。
②易于控制反应进行,反应更充分。(任写一个,合理答案均给1分)
(3)
| 实验操作 | 预期现象与结论 |
| 步骤2:滴入1滴(或少量)品红(1分),再滴入过量2mol/L盐酸,振荡(1分) | 若品红褪色(或有气泡),则“吸收液”中存在 SO32-。(1分) |
| 步骤3:用试管取适量步骤2所得滤液(1分),向其中(或试管中)滴入过量的1mol/LBa(OH)2溶液 [或滴入1滴(或少量)品红溶液,再滴入2-3滴(或过量)的2mol/L盐酸],振荡(1分)。 | 若出现白色沉淀(或品红溶液褪色,或有气泡),则“吸收液”中存在 HSO3-。(1分) |
试题分析:(1)可以使用品红溶液来验证二氧化硫的漂白性,碘单质可以把二氧化硫氧化成正六价的硫而本身被还原成负一价的碘。除了氟之外所有的卤素单质都有这一性质。(2)改进以后的装置少了加热的部分,相对来讲安全程度要好点。再者就是这样的装置可以随时控制二氧化硫的生成量,避免过多的二氧化硫产生从而污染空气。
(3)利用亚硫酸根离子亚硫酸氢根离子的特性来进行检验。

练习册系列答案
相关题目
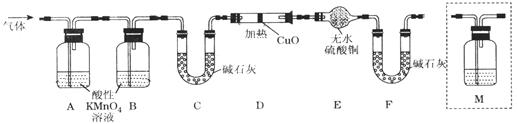
 Fe2(SO4)3+SO2↑+6H2O)。
Fe2(SO4)3+SO2↑+6H2O)。