��Ŀ����
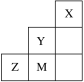
����Ŀ��X��Y��Z��M��Q��R��6�ֶ�����Ԫ�أ���ԭ�Ӱ뾶����Ҫ���ϼ����£�
Ԫ�ش��� | X | Y | Z | M | Q | R |
ԭ�Ӱ뾶/nm | 0.160 | 0.143 | 0.102 | 0.075 | 0.077 | 0.037 |
��Ҫ���ϼ� | ��2 | ��3 | ��6����2 | ��5����3 | ��4����4 | ��1 |
��1��Z��Ԫ�����ڱ��е�λ����_________________________��
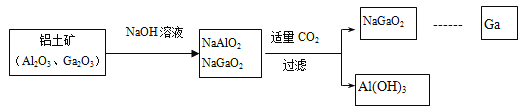
��2��Ԫ��Q��R�γɵĻ�����A�ǹ�ʵ���������A�Ʊ��Ҵ��Ļ�ѧ����ʽ��_______________________��
��3������ͭ��Ԫ��M������������Ӧˮ�����Ũ��Һ������Ӧ�����ӷ���ʽΪ___________________��
��4��Ԫ��X�Ľ����Ա�Ԫ��Y______���ǿ������������
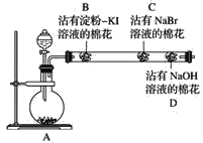
��5��Ԫ��Q��Ԫ��Z�ĺ���Ӱ��������ܣ�������ͼװ��A�ڸ����½�������Ԫ��Q��Ԫ��Zת��ΪQO2��ZO2��

������a�ijɷ���________________���ѧʽ����
����������Ԫ��Z��FeZ����ʽ���ڣ���A�з�Ӧ����ZO2���ȶ��ĺ�ɫ�������Ӧ�Ļ�ѧ����ʽ��_________________________________��
���𰸡��������ڵڢ�A�� CH2=CH2+H2O![]() CH3CH2OH Cu+4H++2NO3-��Cu2++2NO2��+2H2O ǿ O2��SO2��CO2 5O2+3FeS
CH3CH2OH Cu+4H++2NO3-��Cu2++2NO2��+2H2O ǿ O2��SO2��CO2 5O2+3FeS![]() 3SO2+Fe3O4
3SO2+Fe3O4
��������
����Z�Ļ��ϼۣ�6����2���������Ķ�����Ԫ��ֻ��S��������ͬ���ڣ�������ԭ�Ӱ뾶���μ�С��S��ԭ�Ӱ뾶Ϊ0.102���ӱ������ݣ�X�Ļ��ϼ�Ϊ+2��Y�Ļ��ϼ�Ϊ+3����ԭ�Ӱ뾶��S��X��Yֻ��Ϊ�����ڣ�XΪMg��YΪAl����MΪ��5�ۣ�QΪ+4�ۣ�����ԭ�Ӱ뾶��SС������ֻ���Ƕ����ڣ�MΪN��QΪC��R��ԭ�Ӱ뾶��M��Q��С����������Li��ֻ����H��
(1)���ݷ�����ZΪ��Ԫ�����ڱ��е�λ���ǵ������ڵڢ�A�壬�ʴ�Ϊ���������ڵڢ�A�壻
(2) A�ǹ�ʵ�������Ϊ��ϩ������ϩ�Ʊ��Ҵ��Ļ�ѧ����ʽCH2=CH2+H2O![]() CH3CH2OH���ʴ�Ϊ��CH2=CH2+H2O
CH3CH2OH���ʴ�Ϊ��CH2=CH2+H2O![]() CH3CH2OH��
CH3CH2OH��
(3) M������������Ӧˮ����ΪHNO3��ͭ��Ũ���ᷴӦ�����ӷ���ʽΪCu+4H++2NO3-��Cu2++2NO2��+2H2O���ʴ�Ϊ��Cu+4H++2NO3-��Cu2++2NO2��+2H2O��
(4)XΪMg��YΪAl��ͬ���ڣ������ҽ��������μ�����Mg�Ľ�����ǿ���ʴ�Ϊ��ǿ��
(5) ��Ԫ��QΪC��Ԫ��ZΪS���������⣬����a����SO2��CO2���Լ�δ��Ӧ���O2���ʴ�Ϊ��O2��SO2��CO2��
�ڸ������⣬FeS��A��������SO2�ͺ�ɫ���壬����ɫ������һ����Fe������ΪFe3O4����Ӧ�Ļ�ѧ��Ӧ����ʽΪ��5O2+3FeS![]() 3SO2+Fe3O4��
3SO2+Fe3O4��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�