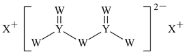
题目内容
【题目】根据原子结构、元素周期表和元素周期律的知识回答下列问题:
(1)A元素次外层电子数是最外层电子数的![]() ,其外围电子轨道表示式是__。
,其外围电子轨道表示式是__。
(2)B是1~36号元素原子核外电子排布中未成对电子数最多的元素,B元素的名称是__,在元素周期表中的位置是__,位于周期表___区,写出基态B原子的核外电子排布式___。
(3)C、N、O、F四种元素第一电离能由大到小的顺序为___,电负性由大到小的顺序为___。
(4)基态Fe2+核外电子排布式为__,Sm的价层电子排布式为4f66s2,Sm3+的价层电子排布式为__。
(5)根据元素As在周期表中的位置预测As的氢化物分子的空间构型为__,其沸点比NH3的__(填“高”或“低”),其判断理由是__。
【答案】![]() 铬 第四周期第ⅥB族 d 1s22s22p63s23p63d54s1或[Ar]3d54s1 F>N>O>C F>O>N>C 1s22s22p63s23p63d6 或[Ar]3d6 4f5 三角锥形 低 氨气分子间含有氢键
铬 第四周期第ⅥB族 d 1s22s22p63s23p63d54s1或[Ar]3d54s1 F>N>O>C F>O>N>C 1s22s22p63s23p63d6 或[Ar]3d6 4f5 三角锥形 低 氨气分子间含有氢键
【解析】
(1)A元素次外层电子数是最外层电子数的![]() ,A元素只能是Ne,则其外围电子轨道表示式是
,A元素只能是Ne,则其外围电子轨道表示式是![]() ,故答案为
,故答案为![]() ;
;
(2) B是1~36号元素原子核外电子排布中未成对电子数最多的元素,B元素是铬,其名称是24号元素铬,在元素周期表中的位置是第四周期第ⅥB族,位于周期表d区,基态Cr原子的核外电子排布式为1s22s22p63s23p63d54s1或[Ar]3d54s1,故答案为:铬;第四周期第ⅥB族;d;1s22s22p63s23p63d54s1或[Ar]3d54s1;
(3) C、N、O、F四种元素中,原子半径r(C)> r(N) >r(O) >r(F),而N原子核外处于2p3半充满状态,更稳定,所以第一电离能F>N>O>C,电负性F>O>N>C,故答案为:F>N>O>C;F>O>N>C;
(4) Fe是26号元素,核外有26个电子,失去两个电子得到Fe2+,基态Fe2+核外电子排布式为1s22s22p63s23p63d6 或[Ar]3d6,Sm的价层电子排布式为4f66s2,失去三个电子得到Sm3+,Sm3+的价层电子排布式为4f5,故答案为:1s22s22p63s23p63d6 或[Ar]3d6;4f5;
(5) As的氢化物分子AsH3与NH3为同一主族的氢化物,结构相似,故AsH3的空间构型为三角锥形,因为NH3分子间含有氢键,所以AsH3的沸点低于氨气,故答案为:三角锥形;低;氨气分子间含有氢键。

 字词句段篇系列答案
字词句段篇系列答案【题目】废弃物的综合利用既有利于节约资源,又有利于保护环境。某工厂对工业污泥中Cr(III)回收与再利用工艺流程如图(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+、Mg2+):

已知:常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH(开始沉淀的pH按金属阳离子浓度为1.0mol·L-1计算)和完全沉淀时溶液的pH,见下表:
阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
开始沉淀时的pH | 1.9 | 7.5 | —— | —— | 4.7 | —— |
沉淀完全时的pH | 3.2 | 9.7 | 11.1 | 8 | 6.7 | 9(>9溶解) |
重铬酸根离子(Cr2O72-)在溶液中存在如下平衡:2CrO42-+2H+![]() Cr2O72-+H2O
Cr2O72-+H2O
(1)该工厂对工业污泥中Cr(+3价)回收与再利用工艺流程中,其中一步存在氢氧化铁的沉淀溶解平衡:Fe(OH)3(s)![]() Fe3+(aq)+3OH-(aq),其溶度积常数表达式为Ksp=__。
Fe3+(aq)+3OH-(aq),其溶度积常数表达式为Ksp=__。
(2)酸浸时,为了提高浸取率可采取的措施是__(至少答一点)。
(3)加入H2O2的作用是__。调节溶液的pH=8是为了除去__离子。
(4)钠离子交换树脂的原理为:Mn++nNaR→MRn+nNa+,被交换的的杂质离子是__。