题目内容
【题目】已知:![]()
![]()
![]() 。25℃时,调节初始浓度为1.0 molL-1 的Na2CrO4溶液的pH,测定平衡时溶液中c(
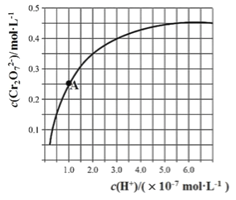
。25℃时,调节初始浓度为1.0 molL-1 的Na2CrO4溶液的pH,测定平衡时溶液中c(![]() )和c(H+),获得如右图所示的曲线。下列说法不正确的是
)和c(H+),获得如右图所示的曲线。下列说法不正确的是
A.平衡时,pH越小,c(![]() )越大
)越大
B.A点CrO![]() 的平衡转化率为50%
的平衡转化率为50%
C.A点CrO![]() 转化为
转化为![]() 反应的平衡常数K=1014
反应的平衡常数K=1014
D.平衡时,若溶液中c(![]() )=c(
)=c(![]() ),则c(H+) > 2.0×10-7 mol·L-1
),则c(H+) > 2.0×10-7 mol·L-1
【答案】D
【解析】
试题分析:A.平衡时,pH越小,氢离子浓度越大,越有利于平衡向正反应方向进行,c(![]() )越大,A正确;B.A点c(
)越大,A正确;B.A点c(![]() )=0.25mol/L,消耗铬酸钠的浓度是0.5mol/L,所以CrO
)=0.25mol/L,消耗铬酸钠的浓度是0.5mol/L,所以CrO![]() 的平衡转化率为50%,B正确;C.A点c(
的平衡转化率为50%,B正确;C.A点c(![]() )=0.25mol/L,c(
)=0.25mol/L,c(![]() )=0.5mol/L,所以CrO
)=0.5mol/L,所以CrO![]() 转化为
转化为![]() 反应的平衡常数K=
反应的平衡常数K=![]() =1014,C正确;D.平衡时,若溶液中c(
=1014,C正确;D.平衡时,若溶液中c(![]() )=c(
)=c(![]() ),根据原子守恒可知c(
),根据原子守恒可知c(![]() )=c(
)=c(![]() )=
)=![]() ,所以根据图像可知c(H+) <2.0×10-7 mol·L-1,D错误,答案选D。
,所以根据图像可知c(H+) <2.0×10-7 mol·L-1,D错误,答案选D。

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
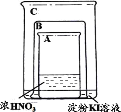
【题目】某同学进行下列实验:
装置 | 操作 | 现象 |
| 将盛有浓硝酸的烧杯A放入盛有淀粉KI溶液的烧杯C中,然后将铜片放入烧杯A后,立即用烧杯B罩住 | 烧杯A液体上方立即出现大量红棕色气体;一段时间后,红棕色气体消失,烧杯A和C中的液体都变成蓝色 |
下列说法合理的是
A.烧杯A中发生反应:3Cu+8HNO3===3Cu(NO3)2+2NO↑+4H2O
B.红棕色气体消失只与NO2和烧杯C中的KI发生反应有关
C.烧杯C中溶液变蓝只与NO2和C中溶液发生反应有关
D.若将铜片换成铁片,则C中的液体也可能变蓝