题目内容
【题目】A(C6H6O)是一种重要的化工原料,广泛用于制造树脂、医药等。
Ⅰ.以A、B为原料合成扁桃酸衍生F的路线如下。
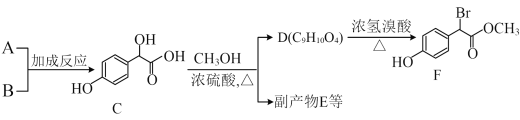
(1)A的名称是____;B的结构简式是____。
(2)C(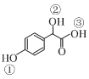 )中①~③羟基氢原子的活性由强到弱的顺序是____。
)中①~③羟基氢原子的活性由强到弱的顺序是____。
(3)D的结构简式是____。
(4)写出F与过量NaOH溶液反应的化学方程式:___________。
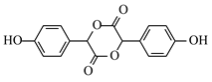
(5)若E分子中含有3个六元环,则E的结构简式是________。
Ⅱ.以A为原料合成重要的医药中间体K的路线如下。
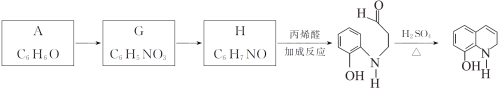
(6)G→H的反应类型是__________。
(7)一定条件下,K与G反应生成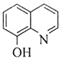 、H和水,化学方程式是__________。
、H和水,化学方程式是__________。
【答案】苯酚 OHC—COOH ③>①>② 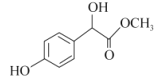
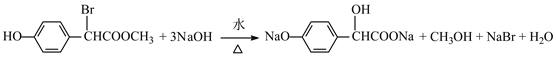
 还原反应 3
还原反应 3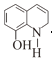 +
+![]()
![]() 3
3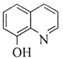 +
+![]() +H2O
+H2O
【解析】
I.A与B发生加成反应产生C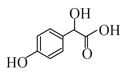 ,根据A的分子式(C6H6O)及C的结构可知A是苯酚,结构简式是
,根据A的分子式(C6H6O)及C的结构可知A是苯酚,结构简式是![]() ,B是OHC-COOH,C与CH3OH在浓硫酸催化下,发生酯化反应产生D为
,B是OHC-COOH,C与CH3OH在浓硫酸催化下,发生酯化反应产生D为 ,D与浓氢溴酸再发生取代反应产生F为
,D与浓氢溴酸再发生取代反应产生F为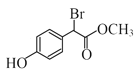 ;若E分子中含有3个六元环,说明2个分子的C也可以发生酯化反应产生1个酯环,得到化合物E,结构简式为
;若E分子中含有3个六元环,说明2个分子的C也可以发生酯化反应产生1个酯环,得到化合物E,结构简式为 。
。
II.A是苯酚![]() ,A与浓硝酸发生苯环上邻位取代反应产生G是
,A与浓硝酸发生苯环上邻位取代反应产生G是![]() ,G发生还原反应产生H为
,G发生还原反应产生H为![]() ,H与丙烯醛CH2=CH-CHO发生加成反应产生
,H与丙烯醛CH2=CH-CHO发生加成反应产生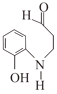 ,
, 与浓硫酸在加热时反应形成K:
与浓硫酸在加热时反应形成K: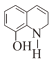 。
。
I.根据上述推断可知:A是![]() ,B是OHC-COOH,D是
,B是OHC-COOH,D是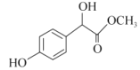 ,E是
,E是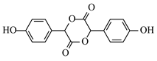 F是
F是 。
。
II.根据上述推断可知G为![]() ,H为
,H为![]() 。
。
(1)A是![]() ,名称为苯酚;B是乙醛酸,B的结构简式是OHC-COOH;
,名称为苯酚;B是乙醛酸,B的结构简式是OHC-COOH;
(2)羧酸的酸性大于苯酚,苯酚的酸性大于醇羟基,因此在物质C(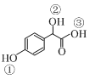 )中①~③羟基氢原子的活性由强到弱的顺序是③>①>②;
)中①~③羟基氢原子的活性由强到弱的顺序是③>①>②;
(3)D的结构简式是 ;
;
(4)F结构简式为 ,含有的酯基与NaOH发生酯的水解反应产生羧酸钠和CH3OH、酚羟基可以与NaOH发生反应产生酚钠、H2O,含有的Br原子可以与NaOH水溶液发生取代反应,Br原子被羟基取代,产生的HBr与NaOH也能发生中和反应,因此F与过量NaOH溶液反应的化学方程式:
,含有的酯基与NaOH发生酯的水解反应产生羧酸钠和CH3OH、酚羟基可以与NaOH发生反应产生酚钠、H2O,含有的Br原子可以与NaOH水溶液发生取代反应,Br原子被羟基取代,产生的HBr与NaOH也能发生中和反应,因此F与过量NaOH溶液反应的化学方程式: +3NaOH
+3NaOH![]()
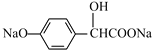 +CH3OH+NaBr+H2O;
+CH3OH+NaBr+H2O;
(5)若E分子中含有3个六元环,则E的结构简式是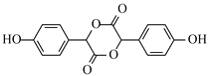 ;
;
(6) G为![]() ,H为
,H为![]() 。G→H的反应类型是硝基被还原为氨基的反应,所以反应类型是还原反应;
。G→H的反应类型是硝基被还原为氨基的反应,所以反应类型是还原反应;
(7)在一定条件下 与
与![]() 发生反应产生
发生反应产生 、
、![]() 、H2O,根据质量守恒定律,可得3
、H2O,根据质量守恒定律,可得3 +
+![]()
![]() 3
3 +
+![]() +H2O。
+H2O。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】能源与材料、信息一起被称为现代社会发展的三大支柱。面对能源枯竭的危机,提高能源利用率和开辟新能源是解决这一问题的两个主要方向。
(1)化学反应速率和限度与生产、生活密切相关,这是化学学科关注的方面之一。某同学为了探究锌与盐酸反应过程中的速率变化,在 400mL 稀盐酸中加入足量的锌粉,用排水法收集反应放出的氢气,实验记录如下(累计值):
时间/min | 1 | 2 | 3 | 4 | 5 |
氢气体积/mL(标况) | 100 | 240 | 464 | 576 | 620 |
①哪一段时间内反应速率最大:____min(填“0~1”或“1~2”或“2~3”或“3~4” 或“4~5”)。
②另一学生为控制反应速率防止反应过快难以测量氢气体积。他事先在盐酸中加入等体积的下列溶液以减慢反应速率但不影响生成氢气的量。你认为可行的是____(填字母序号)。
A.KCl 溶液 B.浓盐酸 C.蒸馏水 D.CuSO4 溶液
(2)如图为原电池装置示意图:
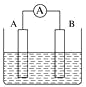
①若 A 为铝,B 为镁,电解质为稀硫酸溶液,则负极材料是_______(填“铝片”或“镁片”)。
②若A为Cu,B 为石墨,电解质为 FeCl3 溶液,工作时的总反应为 2FeCl3+Cu=2FeCl2+CuCl2。写出铜电极的电极反应式:____;若该电池反应消耗了 0.1mol FeCl3, 则转移电子的数目为 _____。
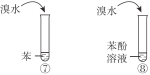
【题目】下列实验内容能达到实验目的的是
实验目的 | 实验内容 | |
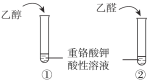
A | 鉴别乙醇与乙醛 |
|
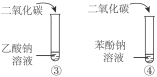
B | 比较乙酸、碳酸、苯酚的酸性 |
|
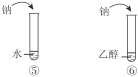
C | 说明烃基对羟基上氢原子活性的影响 | |
D | 说明苯环对取代基上氢原子活性的影响 |
|
A. AB. BC. CD. D