题目内容
【题目】根据信息书写相关反应方程式:
(1)磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。回收废旧磷酸亚铁锂电池正极片[含Al、炭黑、LiFePO4(难溶于水和碱)]中各物质的流程如下图所示:

①写出“碱溶”时的离子方程式:________。
②写出“酸溶”时的化学方程式:________。
③LiFePO4可由Fe2O3、碳粉、LiH2PO4在480℃~900℃时混合共热制得,反应中还有CO生成,写出该反应的化学方程式:________。
(2)羟基自由基(电子式为![]() ,本题用·OH表示)有较强的氧化性,常用于污染物的治理。
,本题用·OH表示)有较强的氧化性,常用于污染物的治理。
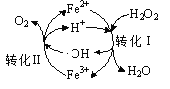
①pH=3时,Fe2+可循环催化H2O2的分解,过程中会产生·OH 中间体,转化过程如右图所示。写出转化Ⅱ的离子方程式:________。
②写出酸性条件下,·OH将水中的乙醛氧化成CO2和H2O的离子方程式:________。
【答案】2Al+2OH-+2H2O=2AlO2-+3H2↑ 6LiFePO4+12H2SO4+2HNO3=3Li2SO4+3Fe2(SO4)3+6H3PO4+2NO↑+4H2O Fe2O3+C+2LiH2PO4![]() 2LiFePO4+CO↑+2H2O 2Fe3++2·OH=2Fe2++O2↑+2H+ 10·OH+CH3CHO=2CO2↑+7H2O
2LiFePO4+CO↑+2H2O 2Fe3++2·OH=2Fe2++O2↑+2H+ 10·OH+CH3CHO=2CO2↑+7H2O
【解析】
(1)①废旧磷酸亚铁锂电池正极片中含Al,可溶解与强碱溶液;
②废旧磷酸亚铁锂电池正极片中含Al、炭黑和LiFePO4,其中Al在“碱溶”过程中完全溶解,因此在“酸溶”过程中溶解的是LiFePO4;
③根据氧化还原反应的规律书写方程式;
(2)①pH=3时,Fe3+氧化·OH生成Fe2+和O2,据此书写离子方程式;
②羟基自由基具有较强的氧化性,能将乙醛氧化为CO2和H2O。
(1)①废旧磷酸亚铁锂电池正极片中含Al,与氢氧化钠溶液反应生成偏铝酸钠和氢气,因此“碱溶”时的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
②“酸溶”过程中溶解的是LiFePO4,LiFePO4与H2SO4和HNO3反应生成Li2SO4、Fe2(SO4)3、H3PO4、NO和H2O,反应方程式为:6LiFePO4+12H2SO4+2HNO3=3Li2SO4+3Fe2(SO4)3+6H3PO4+2NO↑+4H2O;
③LiFePO4可由Fe2O3、碳粉、LiH2PO4在480℃~900℃时混合共热制得,反应中还有CO生成,方程式为:Fe2O3+C+2LiH2PO4![]() 2LiFePO4+CO↑+2H2O;
2LiFePO4+CO↑+2H2O;
(2)①pH=3时,Fe3+氧化·OH生成Fe2+和O2,离子方程式为:2Fe3++2·OH=2Fe2++O2↑+2H+;
②羟基自由基具有较强的氧化性,能将乙醛氧化为CO2和H2O,离子方程式为:10·OH+CH3CHO=2CO2↑+7H2O。