��Ŀ����
����Ŀ���̷��Ǻ���һ�����ᾧˮ�������������ڹ�ũҵ�����о�����Ҫ����;��ij��ѧ��ȤС����̷���һЩ���ʽ���̽�����ش��������⣺
(1)���Թ��м��������̷���Ʒ����ˮ�ܽ⣬�μ�KSCN��Һ����Һ��ɫ�����Ա仯�������Թ���ͨ���������Һ��졣�ɴ˿�֪��______��______��
(2)Ϊ�ⶨ�̷��нᾧˮ��������ʯӢ������(�����˿���K1��K2)(��Ϊװ��A)���أ���Ϊm1 g������Ʒװ��ʯӢ�������У��ٴν�װ��A���أ���Ϊm2g������ͼ���Ӻ�װ�ý���ʵ�顣
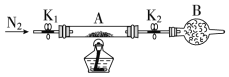
������B��������______��
�ڽ�����ʵ�����������ȷ����______(����)���ظ������������裬ֱ��A���أ���Ϊm3 g��
a.��ȼ�ƾ��ƣ����� b.Ϩ��ƾ��� c.�ر�K1��K2
d.��K1��K2������ͨ��N2 e.����A f.��ȴ������
(3)Ϊ̽�����������ķֽ�����(2)���Ѻ��ص�װ��A������ͼ��ʾ��װ���У���K1��K2������ͨ��N2�����ȡ�ʵ���Ӧ���в�������Ϊ��ɫ��ĩ��
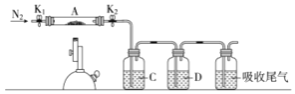
��C��D�е���Һ����Ϊ______(����)��C��D��������ð����
A.NaOH B.Ʒ�� C.ŨH2SO4 D.Ba(NO3)2 E.BaCl2
��д�������������·ֽⷴӦ�Ļ�ѧ����ʽ__________��
���𰸡���Ʒû�б��� �̷����ױ����� (����)����� dabfce E��B 2FeSO4![]() Fe2O3+SO2��+SO3��
Fe2O3+SO2��+SO3��
��������
(1)�������Ӳ��ȶ����ױ������������������������ӣ�
(2)�ٸ���������ͼ�ο��ж��������ƣ�
��ʵ��ʱ��Ϊ����������������Ӧ��ͨ�뵪���ų�װ���еĿ�������ȴʱע��رտ��أ���ȴ�������ٳ������������ı仯��
(3)�����������·ֽ������Fe2O3��SO3��SO2��CΪ�Ȼ�����Һ�����ڼ���SO3��DΪƷ����Һ�������ڼ���SO2��
(1)�μ�KSCN��Һ����Һ��ɫ�����Ա仯����֪��Ʒ��û��Fe3+����Fe2+���ȶ����ױ�������������������Fe3+��������Һ���ɫ��
(2)����������ͼ�ο�֪BΪ����ܣ�
��ʵ��ʱ��Ϊ����Fe2+��������Ӧ��ͨ�뵪�����ų�װ���еĿ�������ȴʱע��رտ��أ���ȴ�������ٳ������������ı仯������ȷ��˳��Ϊdabfce��
(3)��ʵ���Ӧ���в�������Ϊ��ɫ��ĩ��˵������Fe2O3����Ӧ��FeԪ�ػ��ϼ����ߣ�SԪ�ػ��ϼ�Ӧ���ͣ���һ������SO2����֪�����������·ֽ������Fe2O3��SO3��SO2��CΪ�Ȼ��������ڼ���SO3��������Ӧ��SO3+H2O=H2SO4��BaCl2+H2SO4=BaSO4��+2HCl����˿ɹ۲쵽������ɫ������DΪƷ����Һ�������ڼ���SO2���ɹ۲쵽Ʒ����Һ��ɫ��δ��Ӧ��SO2��SO3�ᵼ�´�����Ⱦ���ɸ��ݶ���������������ܹ�������Ӧ���ü�������Һ����ȥSO2��SO3���ų��价����ɵ���Ⱦ���ʺ���ѡ����E��B��
�������������·ֽ������Fe2O3��SO3��SO2���ֽⷴӦ����ʽΪ��2FeSO4![]() Fe2O3+SO2��+SO3����
Fe2O3+SO2��+SO3����

 �¿α�������������ҵ�������γ�����ϵ�д�
�¿α�������������ҵ�������γ�����ϵ�д� ����ν����Ž̲��㽭���̴�ѧ������ϵ�д�
����ν����Ž̲��㽭���̴�ѧ������ϵ�д�����Ŀ����ҵ�ϳɰ��ķ�ӦΪN2(g)��3H2(g)![]() 2NH3(g)����֪���л�ѧ���ļ��ܣ�
2NH3(g)����֪���л�ѧ���ļ��ܣ�
��ѧ�� | ����kJ/mol |
H-H | 436 |
N-H | 391 |
N | 946 |
����˵����ȷ����
A. �÷�ӦΪ���ȷ�ӦB. �÷�Ӧ�з�Ӧ��������������������������
C. ��Ӧ����H��92 kJ��mol��1D. ����1 mol NH3�ų�92 kJ����