��Ŀ����
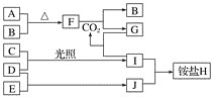
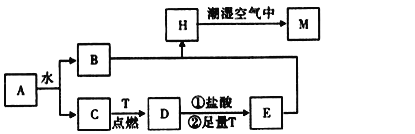
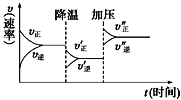
����Ŀ����ͼ��һ����ѧ���̵�ʾ��ͼ��
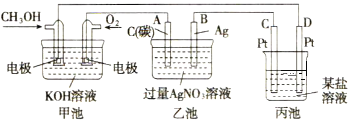
��1��ͼ�м׳���______װ��(��������������ԭ�����)������OH-����______��(����CH3OH������O2��)��
��2��д��ͨ��CH3OH�ĵ缫�ĵ缫��Ӧʽ��_______��
��3�����ҳ����缫�����ֱ�μ�������ɫʯ����Һ���������ĵ缫Ϊ________��(����A������B��)����д���˵缫�ķ�Ӧʽ_______��
��4���ҳ����ܷ�Ӧ�����ӷ���ʽ_________��
��5�������£����ҳ���B(Ag)������������5.40gʱ���ҳص�pH��_______(����ʱ�ҳ�����Һ�����Ϊ500mL)����ʱ����ij�缫����1.60gij����������е�ij����Һ������________(�����)��
A.MgSO4 B.CuSO4 C.NaCl D.KOH
���𰸡�ԭ��� CH3OH CH3OH-6e-+8OH-=CO32-+6H2O A 4H2O-4e-=O2��+4H+ 4Ag++2H2O=4Ag+O2��+4H+ 1 B
��������
(1)ȼ�ϵ������ԭ��أ�ԭ��طŵ�ʱ����Һ���������������ƶ������������ƶ���
(2)ȼ�ϵ����ȼ��ʧ���ӷ���������Ӧ���״�ʧ���Ӻ����������ӷ�Ӧ����̼������Ӻ�ˮ��
(3)�ҳ�����ӵ�Դ�ǵ��أ�������ˮ�õ������������������ӣ������������ӷŵ磬������Һʹ��ɫʯ����Һ��죬���ݵ缫������Һ������Ա仯ȷ����Һ���ĵ缫��
(4)�����������Һʱ�������ӵõ�����������ˮʧ�������������������ӣ��ݴ�д�����ӷ���ʽ��
(5)�������������ӹ�ϵʽ����������Ũ�ȣ��Ӷ�ȷ����Һ��pH���������������������ڽ������˳����н���Ԫ�ش���HԪ�غ��ݴ��������ת�Ƶ��������֪��������������Ԫ����Ҫ�ĵ��ӵ��ڻ�С���ҳ���ת�Ƶ��������ݴ�ȷ�����еĽ���Ԫ�ء�
(1)ȼ�ϵ���ǻ�ѧ��ת��Ϊ���ܵ�װ�ã�����ԭ��أ�ȼ�ϵ���У�Ͷ��ȼ�ϵĵ缫�Ǹ�����Ͷ���������ĵ缫��������ԭ��طŵ�ʱ���������Һ���������������ƶ�������Ͷ�ż״��ĵ缫�ƶ����ʴ�Ϊ��ԭ��أ�CH3OH��
(2)��ȼ�ϵ���У��״�ʧ���Ӻ����������ӷ�Ӧ����̼������Ӻ�ˮ���缫��ӦʽΪ��CH3OH-6e-+8OH-=CO32-+6H2O���ʴ�Ϊ��CH3OH-6e-+8OH-=CO32-+6H2O��
(3)�ҳ�����ӵ�Դ���ڵ��أ�����ԭ���������A������������ԭ��ظ�����B�������������������Һʱ��A�缫��ˮ�õ������������������ӣ��缫��ӦʽΪ4H2O-4e-=O2��+4H+����Һ�����ԣ��μ���ɫʯ����Һ�ʺ�ɫ�� �ʴ�Ϊ��A��4H2O-4e-=O2��+4H+��
(4)�����������Һʱ�������ӵõ�����������ˮʧ�������������������ӣ����ӷ���ʽΪ4Ag++2H2O=4Ag+O2��+4H+���ʴ�Ϊ��4Ag++2H2O=4Ag+O2��+4H+��
(5)���ҳ���B(Ag)������������5.40gʱ����������Ũ��Ϊxmol/L��
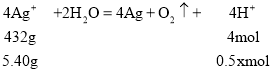
�У�![]() =
=![]() ����ã�x=0.1������Һ��pH=1���������������������ڽ������˳����н���Ԫ�ش���HԪ�غ��ݴ��������ת�Ƶ��������֪��������������Ԫ����Ҫ�ĵ��ӵ��ڻ�С���ҳ���ת�Ƶ�������B������5.40gʱת�Ƶ�����0.05mol��A������þ��þԪ�ش���HԪ��ǰ�����������ϲ������������ʣ��ʴ���B���������ͭ��Һʱ������������1.60gͭ��Ҫת�Ƶ���0.05mol������ȷ��C���Ȼ�������Ԫ�ش�����Ԫ��ǰ�����������ϲ������������ʣ��ʴ���D���������������Һ�൱�ڵ��ˮ�����������������ʣ��ʴ���ѡB���ʴ�Ϊ��1��B��
����ã�x=0.1������Һ��pH=1���������������������ڽ������˳����н���Ԫ�ش���HԪ�غ��ݴ��������ת�Ƶ��������֪��������������Ԫ����Ҫ�ĵ��ӵ��ڻ�С���ҳ���ת�Ƶ�������B������5.40gʱת�Ƶ�����0.05mol��A������þ��þԪ�ش���HԪ��ǰ�����������ϲ������������ʣ��ʴ���B���������ͭ��Һʱ������������1.60gͭ��Ҫת�Ƶ���0.05mol������ȷ��C���Ȼ�������Ԫ�ش�����Ԫ��ǰ�����������ϲ������������ʣ��ʴ���D���������������Һ�൱�ڵ��ˮ�����������������ʣ��ʴ���ѡB���ʴ�Ϊ��1��B��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�����Ŀ���������о������ʣ���H2 ���� ��Na2O2 ��CO2 ��H2SO4 ��Ba(OH)2���� �߰�ˮ ��ϡ���� ������Al2(SO4)3
��1�������ʵķ������д����Ŀհ״���
����� | �ܵ��� | �ǵ���� | ����� |
���ڸ�������� | ___ | ___ | ___ |
��2������ʮ������������������֮��ɷ������ӷ�Ӧ��H++OH-=H2O�������ӷ�Ӧ��Ӧ�Ļ�ѧ����ʽΪ___��
��3�������Ģߵμӵ������Һ�е����ӷ���ʽΪ___��34.2g������ˮ���250mL��Һ��SO42-�����ʵ���Ũ��Ϊ___��
��4������۳�ַ�Ӧ�Ļ�ѧ����ʽΪ��___����ת��NA���ӣ����ɱ������������Ϊ___��
��5����������Ӧ�Ļ�ѧ����ʽΪ��Al+4HNO3=Al(NO3)3+NO��+2H2O���÷�Ӧ����������___���ѧʽ������ԭ���������������ʵ���֮����___������5.4gAl������Ӧʱ��ת�Ƶ��ӵ����ʵ���Ϊ___��