题目内容
12.设NA为阿伏加德罗常数的值,标准状况下O2和N2的混合气体m g含有b个分子,则n g该混合气体在相同状况下所占的体积应是( )| A. | $\frac{22.4nb}{m{N}_{A}}$L | B. | $\frac{22.4mb}{n{N}_{A}}$ L | C. | $\frac{22.4n{N}_{A}}{mb}$ L | D. | $\frac{nb{N}_{A}}{22.4m}$ L |
分析 先求出ng该混合气体含有的分子数,再根据n=$\frac{N}{{N}_{A}}$计算出ng该混合气体物质的量,最后根据V=n×Vm 计算出n g该混合气体在相同状况下所占的体积.
解答 解:根据其组分及其含量相同,所以其质量与分子数成正比,设ng该混合气体含有的分子数为x个,
质量与分子数的比列式为:mg:b=ng:x,
x=$\frac{ng×b}{mg}$=$\frac{nb}{m}$个;
ng该混合气体含有的物质的量为:n=$\frac{N}{{N}_{A}}$=$\frac{\frac{nb}{m}}{{N}_{A}}$mol=$\frac{nb}{m{N}_{A}}$mol,
其体积为:V=n×Vm =$\frac{nb}{m{N}_{A}}$mol×Vm =$\frac{nb}{m{N}_{A}}$mol×22.4l/mol=$\frac{22.4nb}{m{N}_{A}}$L,
故选A.
点评 本题考查了物质的量、质量、气体摩尔体积之间的关系,题目难度不大,灵活运用公式是解题的关键,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
3.能正确解释下列反应原理的离子方程式是( )
| A. | 用NaOH溶液吸收多余的氯气:Cl2+2OH-═Cl-+ClO-+H2O | |
| B. | 用小苏打治疗胃酸过多:CO32-+2H+═CO2↑+H2O | |
| C. | Fe粉加入稀盐酸中制取氢气:2 Fe+6 H+═2 Fe3++3 H2↑ | |
| D. | 氢氧化钡溶液与稀硫酸混合:Ba2++SO42-═BaSO4↓ |
7.向4L容器中充人0.7molSO2和0.4molO2,1s末测得剩余SO2是0.3mol,则 v(O2)( )
| A. | 0.100 mol/(L•min) | B. | 0.025 mol/(L•s) | C. | 0.05 mol/(L•min) | D. | 0.0125 mol/(L•s) |
4.物质在发生化学反应时( )
| A. | 它们的质量一定相等 | |
| B. | 它们的物质的量一定相等 | |
| C. | 它们的质量比等于方程式中化学计量数之比 | |
| D. | 它们物质的量比等于方程式化学计量数之比 |
1.下列离子方程式正确的是( )
| A. | 铁和足量稀硝酸反应:Fe+2H+═Fe2++H2↑ | |
| B. | 碳酸钙和稀硝酸反应:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| C. | 稀硫酸和Ba(OH)2溶液反应:Ba2++H++SO42-+OH-═BaSO4↓+H2O | |
| D. | Cl2和FeCl2溶液反应:Cl2+Fe2+═Fe3++2Cl- |
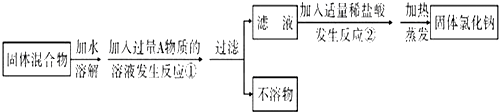
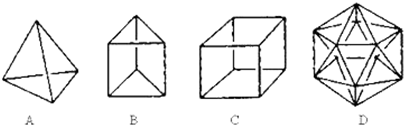
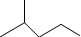 表示的分子式C6H14;名称是2甲基-戊烷.
表示的分子式C6H14;名称是2甲基-戊烷.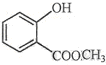 中含有的官能团的名称为羟基、酯基.
中含有的官能团的名称为羟基、酯基.