题目内容
5.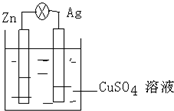 (1)在银锌原电池中,以硫酸铜为电解质溶液,锌为负极,电极上发生的是氧化反应(“氧化”或“还原”).电极反应式为Zn-2e-═Zn2+.
(1)在银锌原电池中,以硫酸铜为电解质溶液,锌为负极,电极上发生的是氧化反应(“氧化”或“还原”).电极反应式为Zn-2e-═Zn2+.(2)银为正极极,电极上发生的是还原反应(“氧化”或“还原”),电极反应式为Cu2++2e-═Cu.
分析 银、锌、硫酸铜溶液构成的原电池中,锌易失电子发生氧化反应而作负极,银作正极,正极上铜离子得电子发生还原反应生成铜,据此分析解答.
解答 解:(1)银、锌、硫酸铜溶液构成的原电池中,锌作负极,负极上锌失电子发生氧化反应生成锌离子进入溶液,电极反应式为Zn-2e-═Zn2+,
故答案为:负;氧化;Zn-2e-═Zn2+;
(2)银作正极,正极上铜了在得电子发生还原反应而析出铜单质,电极反应式为Cu2++2e-═Cu,
故答案为:正;还原;Cu2++2e-═Cu.
点评 本题考查了原电池原理,明确原电池中正负极上得失电子及发生的反应即可解答,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
15.除去下列物质中的杂质(括号内是杂质),能采用先与过量NaOH溶液充分反应再过滤的方法的是( )
| A. | Fe3O4(Al2O3) | B. | KCl(NaCl) | C. | SiO2(CaCO3) | D. | FeCl2溶液(FeCl3) |
16.根据中学化学教材所附元素周期表判断,下列叙述不正确的是( )
| A. | 第15列元素的最高价氧化物的化学式为R2O5 | |
| B. | 第2列元素中肯定没有非金属元素 | |
| C. | L层电子数为奇数的所有元素所在族的序数与元素原子L层电子数相等 | |
| D. | M层电子数为奇数的所有元素所在族的序数与元素原子M层电子数相等 |
13.下列说法中不正确的是( )
| A. | σ键比π键的电子云重叠程度大,形成的共价键强 | |
| B. | 碳碳双键的键能是碳碳单键键能的2倍 | |
| C. | s-s σ键与s-p σ键的电子云形状对称性相同 | |
| D. | N2分子中有一个σ键,2个π键 |
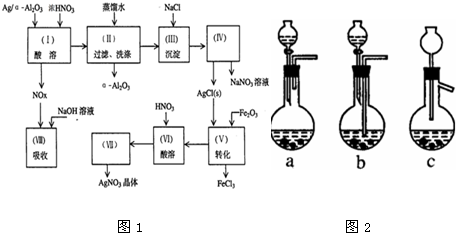
20.V2O5 是一种新型光电材料.某课题组模拟生产V2O5工艺部分流程如下:
Ⅰ.配制偏钒酸钠(NaVO3)溶液
(1)向V2O5 固体中缓慢滴加NaOH溶液,边加热边搅拌至V2O5 固体完全溶解,反应的离子方程式为V2O5+2OH-=2VO3-+H2O.
Ⅱ.沉钒
一定条件下向偏钒酸钠溶液中加入氯化铵溶液,加热、搅拌得到偏钒酸铵沉淀.如图为部分因素对沉钒率的影响.
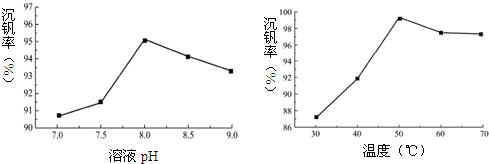
(2)为了提高沉钒率,应调节溶液pH=8.0.已知偏钒酸铵微溶于冷水,可溶于热水,结合图中信息,生成偏钒酸铵沉淀的反应是吸热(填“吸热”或“放热”)反应.
(3)该课题组对影响沉钒率的其他因素(除温度和pH)提出如下假设.
假设一:氯化铵溶液的浓度
假设二:偏钒酸钠溶液浓度
…
(4)结合上述最佳条件设计实验验证假设一,写出实验步骤与结论.
限选试剂:0.5mol/L的偏钒酸钠溶液、1mol/L的氯化铵溶液、蒸馏水,常见实验仪器任选.(提示:沉钒率可用专用仪器测定并计算)
Ⅲ.热分解
(5)偏钒酸铵灼烧产生五氧化二钒,该反应的化学方程式为2NH4VO3$\frac{\underline{\;△\;}}{\;}$2NH3↑+H2O↑+V2O5.
Ⅰ.配制偏钒酸钠(NaVO3)溶液
(1)向V2O5 固体中缓慢滴加NaOH溶液,边加热边搅拌至V2O5 固体完全溶解,反应的离子方程式为V2O5+2OH-=2VO3-+H2O.
Ⅱ.沉钒
一定条件下向偏钒酸钠溶液中加入氯化铵溶液,加热、搅拌得到偏钒酸铵沉淀.如图为部分因素对沉钒率的影响.

(2)为了提高沉钒率,应调节溶液pH=8.0.已知偏钒酸铵微溶于冷水,可溶于热水,结合图中信息,生成偏钒酸铵沉淀的反应是吸热(填“吸热”或“放热”)反应.
(3)该课题组对影响沉钒率的其他因素(除温度和pH)提出如下假设.
假设一:氯化铵溶液的浓度
假设二:偏钒酸钠溶液浓度
…
(4)结合上述最佳条件设计实验验证假设一,写出实验步骤与结论.
限选试剂:0.5mol/L的偏钒酸钠溶液、1mol/L的氯化铵溶液、蒸馏水,常见实验仪器任选.(提示:沉钒率可用专用仪器测定并计算)
| 实验步骤与结论: |
(5)偏钒酸铵灼烧产生五氧化二钒,该反应的化学方程式为2NH4VO3$\frac{\underline{\;△\;}}{\;}$2NH3↑+H2O↑+V2O5.
10.同主族元素的性质较为相似,下列关于同主族元素性质推测正确的是( )
| A. | Li、Na同主族,因为Na在空气中加热生成Na2O2,所以Li在空气中加热生成Li2O2 | |
| B. | F、Cl同主族,因为HCl是强酸,所以HF也是强酸 | |
| C. | Li、Na同主族,因为Na保存在煤油中,所以Li也保存在煤油中 | |
| D. | F、Cl同主族,因为Cl2也是有色气体,所以F2也是有色气体 |
17.下列各组物质中,两种物质所含化学键类型不同的是( )
| A. | H2O和HNO3 | B. | NaCl和NH3 | C. | CaF2和CsF | D. | Cl2和O2 |
 ;
; ;
; .
. ;
; .
.