题目内容
5.实验室制备的CuSO4•5H2O中常含Cu(NO3)2,用重量法测定CuSO4•5H2O的含量.(1)实验步骤为:①称取样品②加水溶解③加氯化钡溶液,沉淀④过滤(其余步骤省略)在过滤前,需要检验是否沉淀完全,其操作是在上层清液中继续滴加加氯化钡溶液,观察有无沉淀产生.
(2)若1.040g试样中含CuSO4•5H2O的准确值为1.015g,而实验测定结果是l.000g 测定的相对误差为-1.5%(-1.48%).
分析 (1)测量固体的含量,要先称量一定质量的固体,经溶解、沉淀、过滤、干燥、称量等操作,要验证是否洗涤完全,向上层清液中继续滴加加氯化钡溶液,若有沉淀产生说明还没有沉淀完全;
(2)相对误差为相对值除以准确值.
解答 解:(1)测量固体的含量,要先称量一定质量的固体,经溶解、沉淀、过滤、干燥、称量等操作,其中沉淀需要洗涤,且要验证是否洗涤完全,向上层清液中继续滴加加氯化钡溶液,若有沉淀产生说明还没有沉淀完全,故答案为:称取样品;在上层清液中继续滴加加氯化钡溶液,观察有无沉淀产生;
(2)相对误差为 ═-1.48%,故答案为:-1.5%(-1.48%).
点评 本题主要考察实验现象等观察、物质的提纯、实验过程设计及有关计算,注意相对误差的计算方法,难度中等.

练习册系列答案
相关题目
11.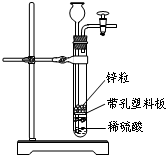 某一兴趣小组准备在实验室中制H2,装置如图所示.可是在实验室中发现酸液不足.为达到实验目的,则可以从长颈漏斗中加入下列试剂中的( )
某一兴趣小组准备在实验室中制H2,装置如图所示.可是在实验室中发现酸液不足.为达到实验目的,则可以从长颈漏斗中加入下列试剂中的( )
 某一兴趣小组准备在实验室中制H2,装置如图所示.可是在实验室中发现酸液不足.为达到实验目的,则可以从长颈漏斗中加入下列试剂中的( )
某一兴趣小组准备在实验室中制H2,装置如图所示.可是在实验室中发现酸液不足.为达到实验目的,则可以从长颈漏斗中加入下列试剂中的( )| A. | NaNO3溶液 | B. | 四氯化碳 | C. | 苯 | D. | Na2CO3溶液 |
16.某未知溶液可能含Cl-、CO32-、Na+、SO42-、Al3+.将溶液滴在蓝色石蕊试纸上,试纸变红.取少量试液,滴加硝酸酸化的氯化钡溶液,有白色沉淀生成;在上层清液中滴加硝酸银溶液,产生白色沉淀.下列判断合理的是( )
| A. | 可能有Cl-和SO42- | B. | 一定有Al3+ 和SO42- | ||
| C. | 可能有Al3+ 和Cl- | D. | 一定没有CO32- |
20.短周期主族元素A、B、C、D、E的原子序数依次增大,其中A与C同主族,A与其它元素不在同一周期,B与D同主族,常温下D的单质为淡黄色固体.下列推断正确的是( )
| A. | 原子半径由小到大的顺序:r(C)<r(D)<r(E) | |
| B. | 元素D、E分别与A形成的化合物的热稳定性:E>D | |
| C. | 元素D的最高价氧化物对应水化物的酸性比E的强 | |
| D. | 元素B分别与A、C形成的化合物中化学键的类型不同 |
10.关于下列装置的说法正确的是( )
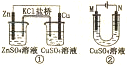

| A. | 装置中盐桥内的K+移向CuSO4溶液 | |
| B. | ①是将电能转变为化学能的装置 | |
| C. | 若装置②用于铁棒镀铜,则N极为铁棒 | |
| D. | 若装置用于电解精炼钢,溶液中Cu2+的浓度保持不变 |
14.结构片段为…-CH2-CH=CH-CH2-…的高分子化合物的单体是( )
| A. | 乙烯 | B. | 乙炔 | C. | 正丁烯 | D. | 1,3-丁二烯 |
7.结构简式为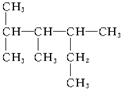 的物质,其名称是( )
的物质,其名称是( )
 的物质,其名称是( )
的物质,其名称是( )| A. | 2,3,4-三甲基己烷 | B. | 1,1,2-三甲基-3-乙基丁烷 | ||
| C. | 2-乙基-3,4-二甲基戊烷 | D. | 3,4,5-三甲基己烷 |
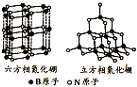 (1)短周期的元素a、b、c、d,原子序数依次增大.a原子的核外电子总数与其电子层数相同,b的基态原子各能级上排布的电子数相同,c的基态原子最高能层有3个未成对电子,d原子的最外层电子数为其内层电子数的3倍.
(1)短周期的元素a、b、c、d,原子序数依次增大.a原子的核外电子总数与其电子层数相同,b的基态原子各能级上排布的电子数相同,c的基态原子最高能层有3个未成对电子,d原子的最外层电子数为其内层电子数的3倍.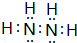 (填电子式).
(填电子式).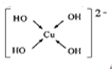 ;
;