题目内容
【题目】以废旧锌锰电池中的黑锰粉(MnO2、MnO(OH)、NH4Cl、少量ZnCl2及炭黑、氧化铁等)为原料制备MnCl2,实现锰的再利用。其工作流程如下:
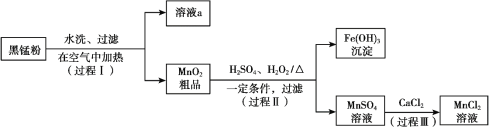
(1)过程Ⅰ,在空气中加热黑锰粉的目的是除炭、氧化MnO(OH)等。O2氧化MnO(OH)的化学方程式是_______。
(2)溶液a的主要成分为NH4Cl,另外还含有少量ZnCl2等。
① 溶液a呈酸性,原因是______。
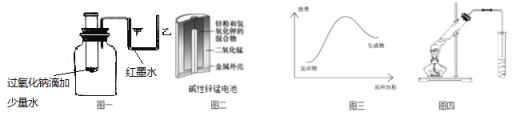
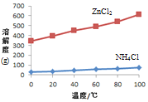
② 根据如图所示的溶解度曲线,将溶液a______(填操作),可得NH4Cl粗品。
③ 提纯NH4Cl粗品,有关性质数据如下:
化合物 | ZnCl2 | NH4Cl |
熔点 | 365℃ | 337.8℃分解 |
沸点 | 732℃ | ------------- |
根据上表,设计方案提纯NH4Cl:________。
(3)检验MnSO4溶液中是否含有Fe3+:取少量溶液,加入_______(填试剂和现象),证明溶液中Fe3+沉淀完全。
(4)探究过程Ⅱ中MnO2溶解的适宜条件。
ⅰ.向MnO2中加入H2O2溶液,产生大量气泡;再加入稀H2SO4,固体未明显溶解。
ⅱ.向MnO2中加入稀H2SO4,固体未溶解;再加入H2O2溶液,产生大量气泡,固体完全溶解。
① 用化学方程式表示ⅱ中MnO2溶解的原因:________。
② 解释试剂加入顺序不同,MnO2作用不同的原因:________。
上述实验说明,试剂加入顺序不同,物质体现的性质可能不同,产物也可能不同。
【答案】4MnO(OH)+O2==4MnO2+2H2O NH4++H2ONH3·H2O+H+(或NH4+水解产生H+) 蒸发浓缩,冷却结晶,过滤 加热NH4Cl粗品至340℃左右,NH4Cl = NH3 + HCl;收集产物并冷却,NH3 + HCl=NH4Cl,得到纯净NH4Cl。 KSCN溶液,不变红 MnO2+H2O2+H2SO4==MnSO4+2H2O+O2↑i中![]() 作催化剂,反应快,
作催化剂,反应快,![]() 只催化分解
只催化分解![]() ii中
ii中![]() 作氧化剂,加入稀
作氧化剂,加入稀![]() 后,
后,![]() 的氧化性增强,被
的氧化性增强,被![]() 还原为
还原为![]() 。
。
【解析】
(1)根据流程图可知,经过过程Ⅰ,得到了MnO2粗品,则O2将MnO(OH)氧化成MnO2,根据得失电子守恒,1molO2得到4mol电子,1molMnO(OH)失去1mol电子,则O2和MnO(OH)的比例为1∶4,再根据原子守恒可配平方程式,答案为4MnO(OH)+O2=4MnO2+2H2O;
(2)①ZnCl2和NH4Cl均为强酸弱碱盐,均会水解,铵根离子水解使溶液呈酸性,答案为NH4++H2ONH3·H2O+H+(或NH4+水解产生H+);
②从曲线可以看出,随着温度的变化,NH4Cl的溶解度几乎没有发生太大的变化,只能蒸发溶剂得到晶体,再进行后续操作,答案为蒸发浓缩,冷却结晶,过滤;
③从表格中数据可以知道,NH4Cl在337.8℃分解,生成NH3和HCl,而此温度下,ZnCl2没有熔化,也没有分解,因此可以利用NH4Cl的分解,收集产物再次合成NH4Cl,答案为加热NH4Cl粗品至340℃左右,NH4Cl = NH3 + HCl;收集产物并冷却,NH3 + HCl=NH4Cl,得到纯净NH4Cl;
(3)Fe3+的检验常用KSCN溶液,如果溶液中有铁离子,生成红色物质;没有Fe3+就不会变红,答案为KSCN溶液,不变红;
(4)从实验ⅰ知道,先加入双氧水,MnO2不溶解,只做催化剂,而通过实验ⅱ可知,先加入硫酸,固体溶解,且有气体冒出,气体为氧气,则MnO2作了氧化剂,双氧水作了还原剂。①固体溶解,且有气体放出,气体为O2,MnO2做氧化剂,H2O2做还原剂,为酸性环境,根据得失电子守恒和原子守恒,配平方程式。答案为MnO2+H2O2+H2SO4=MnSO4+O2↑+2H2O;
②先加入硫酸,溶液为酸性,则酸性条件下,物质的氧化性会增加,答案为ii中![]() 作氧化剂,加入稀
作氧化剂,加入稀![]() 后,
后,![]() 的氧化性增强,被
的氧化性增强,被![]() 还原为MnSO4。
还原为MnSO4。

 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案