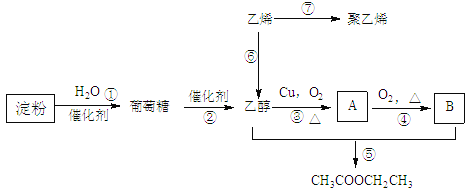
题目内容
【题目】实验室需要配制NaOH溶液和硫酸溶液。
Ⅰ、配制100mL 1.0mol·L-1 NaOH溶液
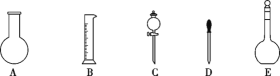
(1)如图所示的仪器中E的名称为___,配制溶液肯定不需要的仪器是___(填序号),还需增加的玻璃仪器有___(填仪器名称)。
(2)在配制NaOH溶液时
①根据计算用托盘天平称取NaOH的质量为___g。
②下列操作对所配溶液浓度的影响是(填“偏高”“偏低”“无影响”)。
操作 | 浓度影响 |
用天平(使用游码)称量时,被称量物与砝码的位置放颠倒了 | ___ |
没有洗涤烧杯和玻璃棒 | ___ |
定容时,仰视读数 | ___ |
容器E未干燥,残余少量水 | ___ |
Ⅱ、配制100mL 0.5mol·L-1 硫酸溶液
用质量分数为98%,密度为1.84g·cm-3的浓硫酸来配制该溶液,该浓硫酸物质的量浓度为___mol·L-1,所需浓硫酸的体积为___mL (计算结果保留一位小数)。
【答案】100mL容量瓶 AC 烧杯、玻璃棒 4.0 偏低 偏低 偏低 无影响 18.4 2.7
【解析】
Ⅰ、(1)由图可知E为容量瓶;配制溶液时需要烧杯、量筒、玻璃棒、胶头滴管、容量瓶;
(2)①利用m=cVM进行计算;
②用天平(使用游码)称量时,被称量物与砝码的位置放颠倒了,称得的试剂质量偏小;没有洗涤烧杯和玻璃棒,溶质的质量减小;定容时,仰视读数,溶液的体积偏大;容量瓶中是否有水对实验无影响;
Ⅱ、利用c=![]() 计算硫酸的浓度;利用稀释定律计算体积。
计算硫酸的浓度;利用稀释定律计算体积。
Ⅰ、(1)由图可知E为容量瓶;配制溶液时需要烧杯、量筒、玻璃棒、胶头滴管、容量瓶,不需要圆底烧瓶和分液漏斗,还需要增加的是烧杯和玻璃棒;
(2)①配制100mL 1.0mol·L-1 NaOH溶液,m=cVM=1.0mol/L×0.1L×40g/mol=4.0g;
②用天平(使用游码)称量时,被称量物与砝码的位置放颠倒了,称得的试剂质量偏小,浓度偏低;没有洗涤烧杯和玻璃棒,溶质的质量减小,浓度偏低;定容时,仰视读数,溶液的体积偏大,浓度偏低;容量瓶中是否有水对实验无影响;
Ⅱ、c(H2SO4)=![]() =
=![]() =18.4mol/L;c(浓溶液)V(浓溶液)=c(稀溶液)V(稀溶液),18.4mol/L×V(浓溶液)= 0.5 mol/L×0.1L,则V(浓溶液)=0.0027L=2.7mL。
=18.4mol/L;c(浓溶液)V(浓溶液)=c(稀溶液)V(稀溶液),18.4mol/L×V(浓溶液)= 0.5 mol/L×0.1L,则V(浓溶液)=0.0027L=2.7mL。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某校化学实验小组在“探究碘水与FeCl2溶液能否反应”的系列实验中发现:在足量的稀KI溶液中,加入1~2滴FeCl3溶液,振荡后溶液呈黄色。
(查阅资料)
碘微溶于水,碘的水溶液颜色随浓度变化呈现黄色或棕色,碘水中含有碘单质;含Fe3+的溶液也呈黄色。
(提出问题)
Fe3+、I2的氧化性强弱情况。
(提出猜想)
(1)甲同学认为氧化性I2>Fe3+,故上述实验现象不是发生化学反应所致,则溶液呈黄色是因为含______;乙同学认为氧化性Fe3+>I2,故上述实验现象是发生化学反应所致,则溶液呈黄色是因为含_______。
(设计实验并验证)
(2)为验证乙同学的观点正确,丙同学选用下面所提供的试剂设计出以下两种方案进行实验,请完成下列表格。供选用的试剂:a.酚酞试液 b.四氯化碳 c.无水酒精 d.KSCN溶液
请你在下列表格中写出丙同学选用的试剂及实验中观察到的现象。(试剂填序号)
试剂 | 实验现象 | |
方案1 | ____________ | ______ |
方案2 | ______ | _________ |
(实验结论)
氧化性:Fe3+>I2。
(拓展应用)
(3)①根据上述实验推测,若在FeI2溶液中通入氯气,首先被氧化的离子是________。
②在100mL FeI2溶液中通入2.24LCl2(标准状况下),溶液中若有![]() 的Fe2+ 被氧化,用离子方程式表示该反应过程:___。
的Fe2+ 被氧化,用离子方程式表示该反应过程:___。