题目内容
15.300ml 0.01mol/L的FeCl3溶液与200mL 0.06mol/L的KCl溶液中,所含Cl-的物质的量浓度之比为( )| A. | 1:1 | B. | 1:2 | C. | 1:3 | D. | 3:2 |
分析 物质的量浓度与溶液的体积无关,先根据溶液中氯离子的物质的量浓度=盐的浓度×化学式中氯离子个数,求出各溶液中Cl-的物质的量浓度,然后求比值.
解答 解:300mL 0.01mol•L-1的FeCl3溶液中Cl-的物质的量浓度为0.01mol•L-1×3=0.03mol•L-1,200mL 0.06mol•L-1的KCl溶液中Cl-的物质的量浓度为0.06mol•L-1,Cl-的物质的量浓度之比为0.03:0.06=1:2,
故选B.
点评 本题考查了溶液中氯离子物质的量浓度的计算,溶液中氯离子的物质的量浓度为盐的浓度与化学式中离子个数的积,与溶液的体积无关.

练习册系列答案
相关题目
5.下列说法正确的是( )
| A. | 乙烯分子与苯分子中碳碳键不同,但二者都能发生加成反应 | |
| B. | 除去甲烷气体中的乙烯可以将混合气体通过盛有足量酸性高锰酸钾溶液的洗气瓶 | |
| C. | 苯的二氯代物有3种,说明苯分子是由6个碳原子以单双键交替结合而成的六元环 | |
| D. | 乙酸和乙醇在浓硫酸作用下可以反应,该反应属于加成反应 |
10.已知甲醛、乙酸和丙酸混合物中,含氧的质量分数为48%,则含碳的质量分数为( )
| A. | 55.43% | B. | 44.57% | C. | 40% | D. | 49% |
7.下列说法正确的是( )
| A. | 在100℃、101 kPa条件下,1 mol液态水汽化时需要吸收40.69 kJ的热量,则H2O(g)═H2O(l)的△H=+40.69 kJ•mol-1 | |
| B. | 已知CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-802.33 kJ•mol-1,则CH4的燃烧热为802.33 kJ | |
| C. | 稀硫酸与0.1 mol•L-1NaOH溶液反应的热化学方程式为:H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJ•mol-1 | |
| D. | 已知S(g)+O2(g)═SO2(s)△H1,S(g)+O2(g)═SO2(g)△H2,则△H2<△H1 |
13.乙烯与乙烷的混合气体共amol,与bmol氧气共存于一密闭容器中,点燃后充分反应,乙烯和乙烷全部消耗完,得到CO和CO2的混合气体和45g水,则下列说法错误的是( )
| A. | 当a=1时,乙烯和乙烷的物质的量之比为1:1 | |
| B. | 当a=1时,且反应后CO和CO2的混合气体的物质的量为反应前氧气的$\frac{2}{3}$时,则b=3 | |
| C. | 当a=1时,且反应后CO和CO2的混合气体的物质的量为反应前氧气的$\frac{2}{3}$时,则CO和CO2的物质的量之比为3:1 | |
| D. | a的取值范围为$\frac{5}{6}$<a<$\frac{5}{4}$ |

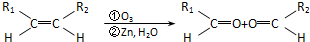
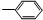 ③-CH═CH2
③-CH═CH2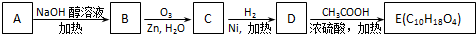
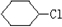 、
、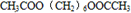 .
.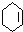
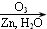
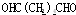 ;
;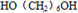 +2CH3COOH$→_{△}^{浓硫酸}$
+2CH3COOH$→_{△}^{浓硫酸}$