题目内容
【题目】氯乙烷跟化合物之间的转化如图所示:
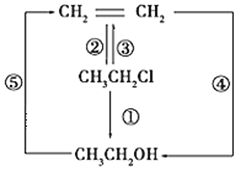
(1)写出各反应的化学方程式①_________,②_________,③__________。
(2)根据上述方程式回答下列问题:
A.上述化学反应的反应类型有__________,__________,__________。
B.用AgNO3溶液通过__________反应可证明卤代烃中含卤元素。
【答案】CH3CH2Cl+ NaOH![]() CH3CH2OH+NaCl CH2=CH2+HCl
CH3CH2OH+NaCl CH2=CH2+HCl![]() CH3CH2Cl CH3CH2Cl+NaOH
CH3CH2Cl CH3CH2Cl+NaOH![]() CH2=CH2↑+NaCl+H2O 取代反应 加成反应 消去反应 ①③
CH2=CH2↑+NaCl+H2O 取代反应 加成反应 消去反应 ①③
【解析】
CH3CH2Cl和NaOH的水溶液共热发生取代反应得到CH3CH2OH,CH2=CH2和HCl在一定条件下发生加成反应生成CH3CH2Cl,CH3CH2Cl和NaOH的醇溶液共热发生消去反应生成CH2=CH2,CH2=CH2和H2O在一定条件下发生加成反应生成CH3CH2OH,CH3CH2OH在浓硫酸作催化剂、170℃条件下发生消去反应生成CH2=CH2,据此分析解答。
(1)通过以上分析知,①的反应方程式为CH3CH2Cl+NaOH![]() CH3CH2OH+NaCl;②的反应方程式为CH2=CH2+HCl
CH3CH2OH+NaCl;②的反应方程式为CH2=CH2+HCl![]() CH3CH2Cl;③的反应方程式为CH3CH2Cl+NaOH
CH3CH2Cl;③的反应方程式为CH3CH2Cl+NaOH![]() CH2=CH2↑+NaCl+H2O;
CH2=CH2↑+NaCl+H2O;
(2)A.通过以上分析可知,发生的反应类型有:取代反应、加成反应、消去反应,故答案为:取代反应;加成反应;消去反应;
B.氯乙烷发生消去反应或取代反应都生成HCl,先向溶液滴加稀硝酸中和未反应的NaOH,再滴加硝酸银溶液检验氯离子,故答案为:①或③。

 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案【题目】Na、Al、Fe、Cu是中学化学中重要的金属元素。它们的单质及其化合物之间有很多转化关系。下表所列物质不能按如图(“→”表示一步完成)关系相互转化的是( )
选项 | A | B | C | D |
|
a | Na | Al | Fe | Cu | |
b | NaOH | Al2O3 | FeCl3 | CuO | |
c | NaCl | Al(OH)3 | FeCl2 | CuSO4 |
A. A B. B C. C D. D
【题目】直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的SO2。
(1)用化学方程式表示SO2形成硫酸型酸雨的反应:______________。
(2)在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是________________________
(3)吸收液吸收SO2的过程中,pH随n(SO3﹣):n(HSO3﹣)变化关系如下表:
n(SO﹣):n(HSO﹣) | 91:9 | 1:1 | 1:91 |
pH | 8.2 | 7.2 | 6.2 |
①上表判断NaHSO3溶液显______性,用化学平衡原理解释:____________
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):____________
a.c(Na+)=2c(SO32-)+c(HSO3-),
b.c(Na+)> c(HSO3-)> c(SO32-)>c(H+)=c(OH-)
c.c(Na+)+c(H+)= c(SO32-)+ c(HSO3-)+c(OH-)
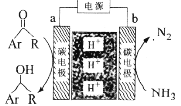
(4)当吸收液的pH降至约为6时,需送至电解槽再生。再生示意图如下:
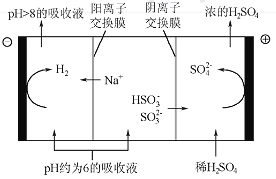
①HSO3-在阳极放电的电极反应式是_______________。
②当阴极室中溶液pH升至8以上时,吸收液再生并循环利用。简述再生原理:__________
【题目】将等物质的量的X、Y气体充入某密闭容器中,在一定条件下,发生如下反应并达到平衡:
X(g)+ 3Y(g) ![]() 2Z(g) △H<0 当改变某个条件并维持新条件直至新的平衡时,下表中关于新平衡与原平衡的比较正确的是
2Z(g) △H<0 当改变某个条件并维持新条件直至新的平衡时,下表中关于新平衡与原平衡的比较正确的是
选项 | 改变条件 | 新平衡与原平衡比较 |
A | 升高温度 | X的转化率变小 |
B | 增大压强 | X的浓度变小 |
C | 充入一定量Y | Y的转化率增大 |
D | 使用适当催化剂 | X的体积分数变小 |
A. A B. B C. C D. D