题目内容
【题目】用酸性氢氧燃料电池为电源电解![]() 溶液,实验装置如图所示.下列关于此装置的说法中,正确的是( )
溶液,实验装置如图所示.下列关于此装置的说法中,正确的是( )

A.燃料电池工作时,负极反应为![]()
B.a极是石墨,b极是铜时,b极的电极反应为:![]()
C.a极是石墨,b极是纯铜时,电解一定时间后两极产生的气体体积都为![]() 标准状况
标准状况![]() ,则原溶液的浓度是
,则原溶液的浓度是![]()
D.a、b两极均是石墨时,若a极产生的气体为![]() 标准状况
标准状况![]() ,则U形管中溶液的PH为
,则U形管中溶液的PH为![]() 体积变化忽略不计
体积变化忽略不计![]()
【答案】C
【解析】
![]() 燃料电池中,负极上燃料失电子发生氧化反应、正极上氧化剂得电子发生还原反应,正极电极反应式为
燃料电池中,负极上燃料失电子发生氧化反应、正极上氧化剂得电子发生还原反应,正极电极反应式为![]() 、负极反应为
、负极反应为![]() ,故A错误;
,故A错误;
B. 通入燃料的电极是负极、通入氧化剂的电极是正极,则a是阳极、b是阴极,阴极上铜离子放电,电极反应为![]() ,故B错误;
,故B错误;
C. a极是石墨,b极是纯铜时,电解一定时间后两极产生的气体体积都为![]() 标准状况
标准状况![]() ,即氢气和氧气的物质的量都是
,即氢气和氧气的物质的量都是![]() ,根据转移电子守恒得
,根据转移电子守恒得![]() ,硫酸铜浓度
,硫酸铜浓度![]() ,故C正确;
,故C正确;
D. a、b两极均是石墨时,若a极产生的气体为![]() 标准状况
标准状况![]() ,a极产生氧气的物质的量
,a极产生氧气的物质的量![]() ,硫酸铜的物质的量未知无法确定氢离子是否放电,所以无法计算溶液的pH,故D错误。
,硫酸铜的物质的量未知无法确定氢离子是否放电,所以无法计算溶液的pH,故D错误。

 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案【题目】某同学进行下列实验:
操作 | 现象 |
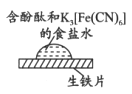
取一块打磨过的生铁片,在其表面滴1滴含酚酞和K3[Fe(CN)6]的食盐水
| 放置一段时间后,生铁片上出现如图所示“斑痕”。边缘处为红色,中心区域为蓝色,在两色环交界处出现铁锈
|
下列对实验现象解释不正确的是
A. 中心区为蓝色的原因是铁失电子被氧化,Fe2+与K3[Fe(CN)6]反应生成蓝色沉淀
B. 边缘处为红色的原因是发生吸氧腐蚀,生成了OH-,使溶液中c(OH-)>c(H+)
C. 边缘处为红色的原因是发生析氢腐蚀,消耗了H+,打破了水的电离平衡,使c(OH-)>c(H+)
D. 交界处出现铁锈的原因是4Fe2++8OH-+O2+2H2O=4Fe(OH)3,Fe(OH)3分解得到铁锈