题目内容
【题目】从含锌矿渣中提取制备锌白(ZnO)有多种方法,其中氨一碳酸氢铵法的优点是成本低。请根据以下材料,回答问题:
材料1:某矿渣的主要成份为ZnO、Fe2O3、PbO、MnO、CuO、SiO2。
材料2:主要反应原理:ZnO+NH4HCO3+3NH3=Zn(NH3)4CO3 + H2O,类似的也可以生成[Cu(NH3)4] 2+、 [Pb(NH3)4]2+这样的络合离子,这些络合离子中的金属元素同样可以被置换出来,同时锰元素会随着金属锌一起进入浸出液中。
材料3:相关阳离子的氢氧化物的Ksp数据如表所示(室温):
阳离子 | Fe2+ | Mn2+ | Pb2+ | Fe3+ | Mn4+ | Pb4+ |
Ksp | 8.0×10-16 | 4.0×10-14 | 1.2×10-15 | 4.0×10-38 | 1.9×10-13 | 3.2×10-66 |
材料4:可选氧化剂与还原剂:
编号 | A | B | C | D |
氧化剂 | 氯气 | 35%过氧化氢 | 过氧化钠 | 酸性高锰酸钾溶液 |
还原剂 | 镁粉 | 铝粉 | 碳粉 | 锌粉 |
材料5:基本工艺(部分):
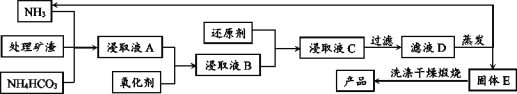
(1)加入氧化剂最好应选择材料4中的_______(填编号);后又加入还原剂的目的是还原溶液中的[Cu(NH3)4]2+、[Pb(NH3)4]2+等离子,请在材料4中选择合适的还原剂写出其中一个离子方程式_______.
(2)对滤液D的蒸发在工艺流程上也叫“蒸氨”,此过程中得到一种碱式盐沉淀物和两种气体,产生的气体可以在经过碱石灰处理后得到纯净而干燥的氨气。固体E经洗涤干燥后,灼烧得到产品,并产生水和CO2。则“蒸氨”过程中发生的化学反应方程式可表述为_______。
【答案】B ![]() 或
或![]()
![]()
【解析】
(1)碳酸氢铵浸取过程中,ZnO、PbO、CuO会溶解,而Fe2O3、SiO2不溶解,而MnO会随金属锌一起进入浸出液中,因此需要采用氧化沉淀法除去锰元素,因氯气氧化性弱于二氧化锰,故不能选用氯气作氧化剂,过氧化钠与高锰酸钾氧化过程中会引入钠离子或钾离子,因此选用双氧水氧化,可节约氧化成本并不会引入杂质,故氧化剂选用双氧水;还原剂的目的是将[Cu(NH3)4] 2+、 [Pb(NH3)4]2+中铜元素、铅元素置换出来,根据金属活动顺序以及不引入杂质可知,还原剂选用锌粉,还原过程中发生的离子反应为:![]() 或
或![]() ,
,
故答案为:B;![]() 或
或![]() ;
;
(2)由题可知,“蒸氨”过程中,生成物为碱式盐沉淀Zn2(OH)2CO3、NH3、CO2,根据元素守恒以及原子守恒可知该过程的化学方程式为:![]() ,
,
故答案为:![]() 。
。

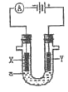
【题目】如图,将甲、乙两个装有不同物质的针筒用导管连接起来,将甲针筒内的物质压到乙针筒内,进行下列实验:

下列说法正确的是( )
实验序号 | 甲针筒内物质 | 乙针筒内物质 | 乙针筒里的现象 |
A | H2S | CuSO4溶液 | 产生黑色沉淀 |
B | H2S | FeSO4溶液 | 产生黑色沉淀 |
C | SO2 | H2S | 出现淡黄色固体 |
D | SO2 | 紫色石蕊溶液 | 先变红后褪色 |
A.AB.BC.CD.D