题目内容
17.下列变化需要加入还原剂才能实现的是( )| A. | Cu→Cu2+ | B. | Cl-→Cl2 | C. | MnO4-→Mn2+ | D. | NH3→NO |
分析 需要加入还原剂才能实现,则选项中氧化剂在反应中元素的化合价降低,以此来解答.
解答 解:A、Cu元素化合价升高,被氧化,应加入氧化剂,故A错误;
B、Cl元素化合价升高,被氧化,应加入氧化剂,故B错误;
C、Mn元素化合价降低,被还原,应加入还原剂,故C正确;
D、N元素化合价升高,被氧化,应加入氧化剂,故D错误,
故选C.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化解答的关键,侧重还原反应的考查,注意从化合价角度分析,题目难度不大.

练习册系列答案
 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
7.下列仪器使用正确的是( )
| A. | 使用漏斗、滤纸、玻璃棒等进行过滤实验 | |
| B. | 用带玻璃塞的试剂瓶盛盐酸 | |
| C. | 在表面皿蒸发浓缩NaCl溶液 | |
| D. | 配制100mL浓度为0.10 mol•L-1Na Cl溶液时,在容量瓶中溶解、定容 |
8.在密闭容器中进行X(g)+4Y2(g)?2Z2(g)+3Q2(g)的反应中,其中X2、Y2、Z2、Q2的开始浓度分别为0.1mol/L、0.4mol/L、0.2mol/L、0.3mol/L,当反应达到平衡后,各物质的浓度不可能是( )
| A. | c(X2)=0.15mol/L | B. | c(Y2)=0.9mol/L | C. | c(Z2)=0.3mol/L | D. | c(Q2)=0.5mol/L |
5.下列叙述正确的是( )
| A. | 1 mol H2O的质量为18 g/mol | |
| B. | CH4的摩尔质量为16 g | |
| C. | 3.01×1023个SO2分子的质量为32g | |
| D. | 标准状况下,1 mol任何物质体积均为22.4 L |
12.下列各组离子中,一定能在溶液中大量共存的是( )
| A. | 在无色溶液中:NH4+、MnO4-、SO42-、CO32- | |
| B. | 在强碱性溶液中:Na+、K+、Cl-、SO32- | |
| C. | 在含大量Ba2+ 的溶液中:H+、Na+、Cl-、OH- | |
| D. | 在酸性溶液中:K+、Fe2+、Cl-、NO3- |
2.下列除去杂质的方法(括号里为少量杂质)中,所用试剂或操作不正确的是( )
| A. | NaHCO3溶液(Na2CO3):通入过量的CO2 | |
| B. | CO2(HCl):将气体通过盛有饱和Na2CO3溶液的洗气瓶 | |
| C. | SiO2(Al2O3):加入稀盐酸再过滤 | |
| D. | FeCl3溶液(FeCl2):通入足量的氯气 |
9.下列电子式书写不正确的是( )
| A. | HCl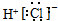 | B. | CaCl2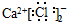 | C. | BaCl2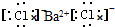 | D. | NaOH 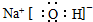 |
6.下列说法正确的是( )
| A. | SO3溶解于水时能导电,所以SO3是电解质 | |
| B. | 离子化合物中不存在独立的分子 | |
| C. | 稀硝酸能导电,所以HNO3溶液属于电解质 | |
| D. | 熔融时能导电的物质一定是电解质 |
2.A(g)+B(g)?3C(g),图中甲、乙、丙分别表示在不同的条件下生成物C在反应混和物中的百分含量(C%)和反应时间(t)的关系.有关图象的说法正确的是( )
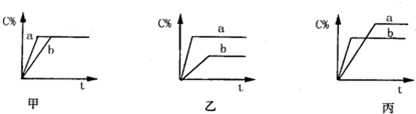

| A. | 若甲图中两条曲线分别表示有催化剂和无催化剂时的情况,则b表示有催化剂的情况 | |
| B. | 若乙图中a曲线表示200℃、b曲线表示100℃时的情况,则反应的正反应是放热反应 | |
| C. | 若丙图中两条曲线分别表示不同压强下的情况,则b曲线是表示压强较大的情况 | |
| D. | 若丙图中两条曲线分别表示不同温度下的情况,则a曲线是表示温度较大的情况 |