题目内容
【题目】钪及其化合物具有许多优良的性能,在宇航、电子、超导等方面有着广泛的应用。从钛白工业废酸(含钪、钛、铁、锰等离子)中提取氧化钪(Sc2O3)的一种流程如下:
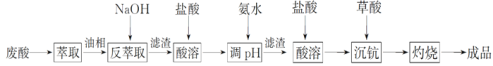
回答下列问题:
(1)洗涤“油相”可除去大量的钛离子。洗涤水是用93%的硫酸、27.5%的双氧水和水按一定比例混合而成。混合的实验操作是______________________________。
(2)先加入氨水调节pH=3,过滤,滤渣主要成分是__________;再向滤液加入氨水调节pH=6,滤液中Sc3+的浓度为_____________。(已知:Ksp[Mn(OH)2]=1.9×10-13、Ksp[Fe(OH)3]=2.6×10-39,Ksp[Sc(OH)3]=9.0×10-31)
(3)用草酸“沉钪”。25 ℃时pH=2的草酸溶液中![]() =__________(保留两位有效数字)。写出“沉钪”得到草酸钪的离子方程式__________________________________。[已知Ka1(H2C2O4)=5.9×10-2,Ka2(H2C2O4)=6.4×10-5]
=__________(保留两位有效数字)。写出“沉钪”得到草酸钪的离子方程式__________________________________。[已知Ka1(H2C2O4)=5.9×10-2,Ka2(H2C2O4)=6.4×10-5]
(4)草酸钪“灼烧”氧化的化学方程式为______________________________________________。
(5)废酸中含钪量为15 mg·L-1,V L废酸最多可提取Sc2O3的质量为____________。
【答案】 将浓硫酸沿烧杯内壁慢慢注入水中,并用玻璃棒不断搅拌,冷却后再慢慢注入 H2O2中,并不断搅拌 Fe(OH)3 9.0×10-7mol·L-l 3.8×10-2 2Sc3++ 3H2C2O4===Sc2(C2O4)3↓+ 6H+ 2Sc2(C2O4)3+3O2![]() 2Sc2O3+12CO2 0.023V g
2Sc2O3+12CO2 0.023V g
【解析】
(1)不同的液体在混合时,一般先加密度较小,易挥发的,后加密度大的、难挥发的,若混合时放热,则最后加受热易分解的,因此,混合的实验操作是将浓硫酸沿烧杯内壁慢慢注入水中,并用玻璃棒不断搅拌,冷却后再慢慢注入 H2O2中,并不断搅拌;(2)废酸中含钪、钛、铁、锰等离子,洗涤“油相”已除去大量的钛离子,根据Ksp[Mn(OH)2]=1.9×10-13、Ksp[Fe(OH)3]=2.6×10-39,Ksp[Sc(OH)3]=9.0×10-31,可以求出余下三种离子沉淀完全(离子浓度小于10-5mol/L)的pH,发现锰离子沉淀完全时pH约为10,钪离子沉淀完全时pH约为5,而铁离子沉淀完全时pH约为4,所以先加入氨水调节pH=3,过滤,滤渣主要成分是Fe(OH)3;再向滤液加入氨水调节pH=6,此时溶液中c(OH-)=10-8mol/L,滤液中Sc3+的浓度为![]() ;(3) 25 ℃时pH=2的草酸溶液中
;(3) 25 ℃时pH=2的草酸溶液中![]() =
=![]() =
=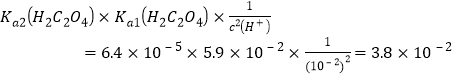 , “沉钪”得到草酸钪的离子方程式为2Sc3++ 3H2C2O4===Sc2(C2O4)3↓+ 6H+;(4)草酸钪“灼烧”氧化的化学方程式为2Sc2(C2O4)3+3O2
, “沉钪”得到草酸钪的离子方程式为2Sc3++ 3H2C2O4===Sc2(C2O4)3↓+ 6H+;(4)草酸钪“灼烧”氧化的化学方程式为2Sc2(C2O4)3+3O2![]() 2Sc2O3+12CO2;(5)废酸中含钪量为15 mg·L-1,则V L废酸中含钪的质量为15
2Sc2O3+12CO2;(5)废酸中含钪量为15 mg·L-1,则V L废酸中含钪的质量为15![]() ,所以最多可提取Sc2O3的质量为
,所以最多可提取Sc2O3的质量为![]() 。
。