题目内容
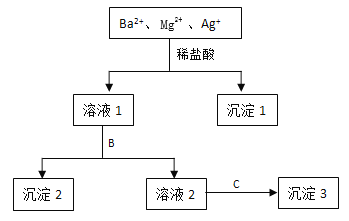
【题目】卤水中蕴含着丰富的镁资源,就MgCl2粗产品的提纯、镁的冶炼过程回答下列问题:已知MgCl2粗产品的溶液中含有Fe2+、Fe3+和Al3+. 表是生成氢氧化物沉淀的pH:
物质 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mg(OH)2 |
开始沉淀pH | 2.7 | 8.1 | 3.8 | 9.5 |
完全沉淀pH | 3.7 | 9.6 | 4.8 | 11.0 |
(1)把MgCl2粗产品的溶液中的Fe2+转化为Fe3+,最适宜选用的物质是____(填序号,下同),加入______调节溶液的pH,充分反应后过滤,可得MgCl2溶液.
a.KMnO4 b.H2O2 c.MgO d.NaOH
(2)若除去溶液中的杂质离子,调节溶液的pH范围为:___________。
(3)由MgCl2溶液获得MgCl2固体的操作是:__________________。
(4)已知:Ksp[BaSO4]=1×10-10,Ksp[BaSO3]=5×10-7。把部分被空气氧化的Na2SO3溶液的pH调为10,向溶液中滴加BaCl2溶液使SO42-沉淀完全[c(SO42-)≤1×10-6mol·L-1],此时溶液中c(SO32-)≤__________mol·L-1。
【答案】 b c 4.8≤pH<9.5 将MgCl2溶液在HCl气流的氛围中加热蒸干 0.005
【解析】(1)把MgCl2粗产品溶液中的Fe2+转化为Fe3+,可加入氧化剂,一般选用H2O2、Cl2,不宜选用KMnO4,会引入新杂质;Fe2+转化为Fe3+后,调节溶液pH使Fe3+完全转化为沉淀,过滤除去;加入的试剂不能引入新的杂质,应选择氧化镁,也可用碳酸镁,不宜使用NaOH,NaOH为强碱,操作过程中,不易控制使用量,且会引入新杂质Na+。
故答案为:b;c;
(2)根据表格可知,pH应调至3.7~9.5之间,为使得Fe3+沉淀完全,pH应大于或等于3.7,而不能使Mg2+沉淀,所以pH应小于9.5。
故答案为:4.8≤pH<9.5;
(3)MgCl2溶液中存在水解,水解方程式为MgCl2+2H2O Mg(OH)2+2HCl,如果直接加热MgCl2溶液,会促进Mg2+水解和HCl挥发,蒸干后得到Mg(OH)2。通入HCl可以抑制Mg2+水解,所以应在HCl气流的氛围中加热蒸干获得MgCl2晶体。
故答案为:将MgCl2溶液在HCl气流的氛围中加热蒸干;
(4)根据Ksp[BaSO4]=c(Ba2+)c(SO42-),当SO42-沉淀完全时,c(Ba2+)= =
=![]() =10-4mol/L,则溶液中SO32-的最大浓度c(SO32-)=
=10-4mol/L,则溶液中SO32-的最大浓度c(SO32-)= =
=![]() =0.005 mol/L。
=0.005 mol/L。
故答案为:0.005。