题目内容
【题目】表1是元素周期表的一部分:
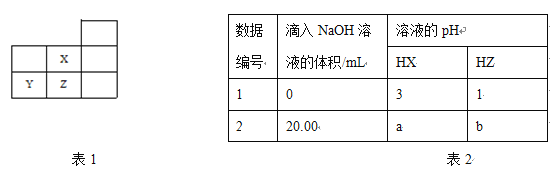
25℃时,用浓度为0.1000 molL-1的氢氧化钠溶液分别滴定20.00mL浓度均为0.1000 molL-1的两种酸HX、HZ(忽略体积变化),实验数据如表2,下列判断正确的是
A. 通过分析可得表格中a <7,b=7
B. 将上述的HZ溶液稀释100倍后pH比HX溶液的pH大
C. 由于Z元素的非金属性比Y强,所以Z氢化物的酸性较强
D. 0.1000 molL-1 Na2Y的水溶液中:c(Y2-) + c(HY-) + c(H2Y) = 0.1000 molL-1
【答案】D
【解析】A. 由HX溶液的pH值可得,HX为弱电解质,则NaX的水溶液pH值大于7,A错误;B. HZ属于强电解质,稀释100倍后,其pH值增加至3,与HX溶液pH值相同,B错误;C. 氢化物酸性取决于电离出氢离子的难度,而不是非金属性强弱的比较,C错误;D. 根据物料守恒,Y元素的物质的量浓度总和等于加入的Na2Y的物质的量浓度,D正确。故选择D。

 名师金手指领衔课时系列答案
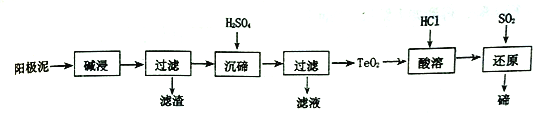
名师金手指领衔课时系列答案【题目】铜镉渣主要含锌、铜、铁、铬(Cd)、钴(Co)等单质。湿法炼锌产生的铜镉渣用于生产金属镉的工艺流程如下:
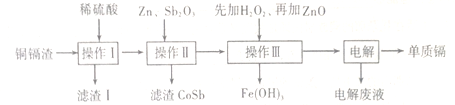
下表列出了相关金属离子生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1mol·L-1)
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 |
开始沉淀的pH | 1.5 | 6.5 | 7.2 |
沉淀完全的pH | 3.3 | 9.9 | 9.5 |
(1)酸浸时粉碎铜镉渣的目的是_______________________。
(2)操作Ⅰ产生的滤渣主要成分为___________________(填化学式)。
(3)①操作Ⅲ中先加入适量H2O2,发生反应的离子方程式为____________________。
②再加入ZnO控制反应液的pH,pH范围为______________,判断依据是_______________。
③若加入的H2O2不足,加入ZnO后所得的电解液中会含有Fe元素。
请设计实验方案加以鉴别___________________________。
(4)处理含镉废水常用加入碳酸钙实现沉淀转化,该沉淀转化的反应方程式为____________。除去工业废水中的Cd2+时,若反应达到平衡后溶液中c(Ca2+)=0.1mol·L-1,溶液中c(Cd2+)=_____mol·L-1 (已知25℃ ,Ksp(CdCO3)=5.6×10-12, Ksp(CaCO3)=5.6×10-9)。
【题目】卤水中蕴含着丰富的镁资源,就MgCl2粗产品的提纯、镁的冶炼过程回答下列问题:已知MgCl2粗产品的溶液中含有Fe2+、Fe3+和Al3+. 表是生成氢氧化物沉淀的pH:
物质 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mg(OH)2 |
开始沉淀pH | 2.7 | 8.1 | 3.8 | 9.5 |
完全沉淀pH | 3.7 | 9.6 | 4.8 | 11.0 |
(1)把MgCl2粗产品的溶液中的Fe2+转化为Fe3+,最适宜选用的物质是____(填序号,下同),加入______调节溶液的pH,充分反应后过滤,可得MgCl2溶液.
a.KMnO4 b.H2O2 c.MgO d.NaOH
(2)若除去溶液中的杂质离子,调节溶液的pH范围为:___________。
(3)由MgCl2溶液获得MgCl2固体的操作是:__________________。
(4)已知:Ksp[BaSO4]=1×10-10,Ksp[BaSO3]=5×10-7。把部分被空气氧化的Na2SO3溶液的pH调为10,向溶液中滴加BaCl2溶液使SO42-沉淀完全[c(SO42-)≤1×10-6mol·L-1],此时溶液中c(SO32-)≤__________mol·L-1。