题目内容
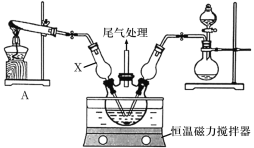
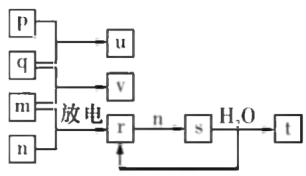
【题目】有关催化剂的催化机理等问题可以从“乙醇催化氧化实验”得到一些认识,某教师设计了如图所示装置(夹持装置等已省略),其实验操作为:先按图安装好装置,关闭活塞a、b、c,在铜丝的中间部分加热片刻,然后打开活塞a、b、c,通过控制活塞a和b,而有节奏(间歇性)地通入气体。在M处观察到明显的实验现象。试回答以下问题:
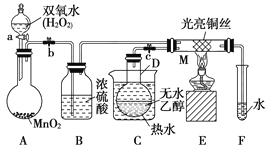
(1)写出A中发生反应的化学方程式:_____________________;B的作用是____________________;C中热水的作用是_________________________________________。
(2)写出M处发生反应的化学方程式为_________________________。
(3)从M管中可观察到的现象为_______________________,从中可认识到该实验过程中催化剂________(填“参加”或“不参加”)化学反应,还可以认识到催化剂起催化作用需要一定的________。
(4)实验进行一段时间后,如果撤掉酒精灯,反应________(填“能”或“不能”)继续进行,其原因是_________________________________。
【答案】2H2O2![]() 2H2O+O2↑ 干燥O2 使D中乙醇变为蒸气进入M中参加反应 2CH3CH2OH+O2
2H2O+O2↑ 干燥O2 使D中乙醇变为蒸气进入M中参加反应 2CH3CH2OH+O2![]() 2CH3CHO+2H2O 受热部分的铜丝由于间歇性地鼓入氧气而交替出现变黑、变红的现象 参加 温度 能 乙醇的催化氧化反应是放热反应,反应放出的热量能维持反应继续进行
2CH3CHO+2H2O 受热部分的铜丝由于间歇性地鼓入氧气而交替出现变黑、变红的现象 参加 温度 能 乙醇的催化氧化反应是放热反应,反应放出的热量能维持反应继续进行
【解析】
(1)A中是过氧化氢在二氧化锰催化作用下生成水和氧气,反应的化学方程式为2H2O2![]() 2H2O+O2↑;B是吸收氧气中的水蒸气;C是加热乙醇得到乙醇蒸气进入M,故答案为:2H2O2
2H2O+O2↑;B是吸收氧气中的水蒸气;C是加热乙醇得到乙醇蒸气进入M,故答案为:2H2O2![]() 2H2O+O2↑;干燥O2;使D中乙醇变为蒸气进入M中参加反应;
2H2O+O2↑;干燥O2;使D中乙醇变为蒸气进入M中参加反应;
(2)M处发生的反应是乙醇的催化氧化反应生成乙醛,反应的化学方程式为:2CH3CH2OH+O2![]() 2CH3CHO+2H2O,
2CH3CHO+2H2O,
故答案为:2CH3CH2OH+O2![]() 2CH3CHO+2H2O;
2CH3CHO+2H2O;
(3)铜丝做催化剂,和氧气反应生成氧化铜,和乙醇反应又生成铜,热部分的铜丝由于间歇性地鼓入空气而交替出现变黑,变红的现象;催化剂参加反应过程,催化作用需要一定的温度,
故答案为:受热部分的铜丝由于间歇性地鼓入空气而交替出现变黑,变红的现象;参加;
(4)如果撤掉酒精灯,反应能继续进行;因为 乙醇的催化氧化反应是放热反应,反应放出的热量维持反应继续进行