题目内容
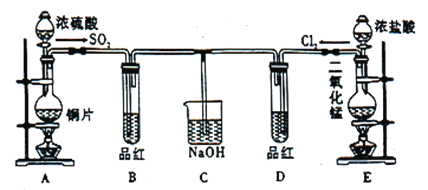
【题目】有A、B、C、D、E、F六种前四周期元素,它们的原子序数依次增大。A、D同主族,A元素的原子最外层p能级的电子数等于次外层的电子总数,C原子最外层中有两个未成对的电子且与A同周期;C元素可分别与A、B、D、E生成RC2型化合物,并知EC2中E与C的质量比为1/1;F能形成红色(或砖红色)和黑色的两种氧化物。根据以上条件,回答下列问题:
(1)请写出F元素的名称 ___________F元素电子排布式___________________________
(2)在EC2分子中,E原子的杂化轨道类型为_________,分子的空间构型为 _______;
(3)H2E和H2C2的主要物理性质比较如下:
熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
H2E | 187 | 202 | 2.6 |
H2C2 | 272 | 423 | 以任意比互溶 |
H2E和H2C2的相对分子质量基本相同,造成上述几种物理性质差异的主要原因 _____________ 。
(4)元素A的一种氢化物是重要的化工原料,常把该氢化物的产量作为衡量石油化工发展水平的标志。有关该氢化物分子的说法正确的是 (_______________)
A.分子中含有分子间氢键 C.只含有4个sp-s的σ键和1个p-p的π键
B.属于含有极性键的非极性分子 D.该氢化物分子中A原子采用sp2杂化
(5)B和F形成某种化合物的晶胞结构如右图所示(每个球均表示1个原子,其中B显-3价),则其化学式为 __________。F的常见离子和B的最简单氢化物形成的配离子的名称为___________,其水溶液颜色为________________。

![]()
【答案】 铜 1s22s22p63s23p63d104s1或[Ar]3d104s1 sp2 V形或角形 H2O2分子间存在氢键,与水分子可形成氢键 B、D Cu3 N 四氨合铜离子 深蓝色
【解析】(1)F能形成红色(或砖红色)和黑色的两种氧化物,根据现象知红色氧化物为氧化亚铜,黑色氧化物为氧化铜,所以知F为Cu, F元素的名称 为铜,F元素电子排布式为:1s22s22p63s23p63d104s1。
(2)由A、B、C、D、E、F六种前四周期元素,C元素可分别与A、B、D、E生成RC2型化合物,并知EC2中E与C的质量比为1/1知EC2为SO2,所以C为O,E为S ,S原子的杂化轨道类型为sp2,分子的空间构型为 V形。
(3) 根据分析知H2E为H2S,H2C2为H2O2,,相对分子质量基本相同,但因为H2O2分子间存在氢键,与水分子可形成氢键,H2S没有,所以造两者物理性质有差异。本题答案:H2O2分子间存在氢键,与水分子可形成氢键 。
(4)由上述分析知C为氧元素,C与A同周期,A元素的原子最外层p能级的电子数等于次外层的电子总数,知A为C。A的一种氢化物是重要的化工原料,常把该氢化物的产量作为衡量石油化工发展水平的标志知A的氢化物为乙烯,结构式为![]() ,可以知道分子中含有
,可以知道分子中含有![]() 非极性键和
非极性键和![]() 极性键,为平面形分子,含有5个
极性键,为平面形分子,含有5个![]() 键和1个
键和1个![]() 键,每个C形成3个
键,每个C形成3个![]() 键,为
键,为![]() 杂化,因此,本题正确答案是:BD。
杂化,因此,本题正确答案是:BD。
(5)有上述分析知道:B为氮元素,F为铜元素,由晶胞的结构和B为-3价,知其化学式为Cu3 N。F的常见离子为Cu2+,B的最简单氢化物为NH3,两者形成形成的配离子为:[Cu(NH3)4] 2+其名称为:四氨合铜离子,其水溶液颜色为深蓝色。答案:四氨合铜离子,深蓝色。

 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案