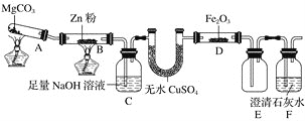
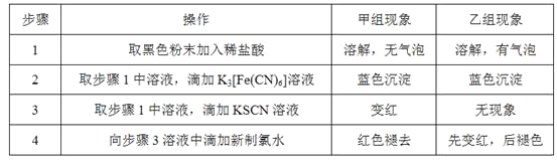
题目内容
【题目】Ⅰ.利用甲烷催化还原NOx消除氮氧化物的污染
①CH4(g)+4NO2(g)![]() 4NO(g)+CO2(g)+2H2O(g) ΔH1=-574kJ·mol-1
4NO(g)+CO2(g)+2H2O(g) ΔH1=-574kJ·mol-1
②CH4(g)+4NO(g)![]() 2N2(g)+CO2(g)+2H2O(g) ΔH2=-1 160kJ·mol-1
2N2(g)+CO2(g)+2H2O(g) ΔH2=-1 160kJ·mol-1
③CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g) ΔH3=-867kJ·mol-1
N2(g)+CO2(g)+2H2O(g) ΔH3=-867kJ·mol-1
(1)如果三个反应的平衡常数依次为K1、K2、K3,则K3=___(用K1、K2表示)。
(2)在2L恒容密闭容器中充入1molCH4和2molNO2进行反应③,CH4的平衡转化率α(CH4)与温度和压强的关系如图所示。
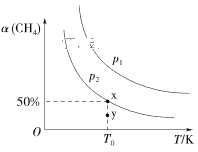
①若容器中的压强为p2,y点:v正____(填“大于”“等于”或“小于”)v逆。
②x点对应温度下反应的平衡常数K=___。
Ⅱ.甲烷蒸气转化法制H2的主要反应为:CH4(g)+H2O(g)![]() CO(g)+3H2(g)
CO(g)+3H2(g)
(3)在恒容密闭容器中充入2 mol CH4和H2O(g)的混合气体,且CH4和H2O(g)的物质的量之比为x,相同温度下达到平衡时测得H2的体积分数φ(H2)与x的关系如图所示。
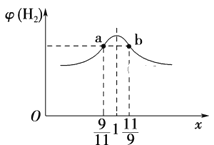
则CH4的转化率:a点____(填“>”“=”或“<”,下同)b点,CH4(g)的浓度:a点_____b点,氢气的产率:a点____b点。
Ⅲ.(4)根据以下三个热化学方程式:2H2S(g)+3O2(g)=SO2(g) +2H2O(l) ΔH=-Q1kJ·mol-1,2H2S(g)+O2(g)= S(s)+2H2O(l) ΔH=-Q2kJ·mol-1,2H2S(g)+O2(g)= S(s)+2H2O(g) ΔH=-Q3kJ·mol-1,判断Q1、Q2、Q3的大小关系是___。
【答案】![]() 大于 0.25 > = = Q1>Q2>Q3
大于 0.25 > = = Q1>Q2>Q3
【解析】
(1)依据已知的热化学方程式利用盖斯定律构造CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g),然后根据关系式得到平衡常数的关系;
(2)①y趋向平衡时,甲烷的转化率应增大;
②x点甲烷的转化率为50%,以此计算平衡时各物质的浓度,可计算平衡常数;
(3)两种反应物存在,增加其中一种反应物的量,能使另一种反应物的转化率提高,根据反应方程式分析a、b两点CH4和H2O的浓度关系和氢气的产率大小;
(4)依据焓变的含义和反应物质的聚集状态变化,反应的进行程度进行分析判断,结合盖斯定律的内容分析物质转化的能量变化。
(1)①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g);②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1160kJmol-1;由盖斯定律![]() ×(①+②)得到CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g),已知三个反应的平衡常数依次为K1、K2、K3,则K3=
×(①+②)得到CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g),已知三个反应的平衡常数依次为K1、K2、K3,则K3=![]() =
=![]() ;
;
(2)①y趋向平衡时,甲烷的转化率应增大,即反应正向进行,v正大于v逆;
②在恒容(2L) 密闭容器中充入1molCH4和2moINO2进行(1)中反应,x点甲烷的转化率为50%,
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)
起始(mol/L) 0.5 1 0 0 0
转化(mol/L) 0.25 0.5 0.25 0.25 0.5
平衡(mol/L) 0.25 0.5 0.25 0.25 0.5
则K=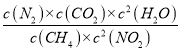 =
=![]() =0.25;
=0.25;
(3)两种反应物存在,增加其中一种反应物的量,能使另一种反应物的转化率提高,a点H2O的含量相对较大,所以a点CH4的转化率更高;根据反应方程式分析,CH4和H2O是按照1:1反应的,a点CH4和H2O的物质的量之比为9:11,b点CH4和H2O的物质的量之比为11:9,所以二者平衡时a点CH4的浓度等于b点H2O(g)的浓度;由于二者CH4和H2O按物质的量1:1反应,所以交换二者的起始充入量之比不改变化学平衡,即达到平衡时氢气的产率a点等于b点;
(4)①2H2S(g)+3O2(g)=2SO2(g)+2H2O(1)△H=-Q1KJ/mol,②2H2S(g)+O2(g)=2S(g)+2H2O(1)△H=-Q2KJ/mol,③2H2S(g)+O2(g)=2S(g)+2H2O(g)△H=-Q3KJ/mol;反应②③相比,生成气态水和生成液态水相比,生成液态水放出的热量多,所以Q2>Q3;反应①②相比,②反应生成的单质硫转化为二氧化硫时放出热量,所以Ql>Q2;综上所述Q1、Q2、Q3三者大小关系为:Ql>Q2>Q3。

【题目】I. CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决温室效应的有效途径。
已知反应Fe(s)+CO2(g)![]() FeO(s)+CO(g)的平衡常数为K1;
FeO(s)+CO(g)的平衡常数为K1;
反应Fe(s)+H2O(g)![]() FeO(s)+H2(g)的平衡常数为K2。
FeO(s)+H2(g)的平衡常数为K2。
在不同温度时K1、K2的值如下表:
温度 | K1 | K2 |
973K | 1.47 | 2.38 |
1173K | 2.15 | 1.67 |
(1)推导反应CO2(g)+H2(g)![]() CO(g)+H2O(g)的平衡常数K与K1、K2的关系式:_________,判断该反应是_____________反应(填“吸热”或“放热”)。
CO(g)+H2O(g)的平衡常数K与K1、K2的关系式:_________,判断该反应是_____________反应(填“吸热”或“放热”)。
II. T1温度下,体积为2L的恒容密闭容器,加入4.00molX,2.00molY,发生化学反应 2X(g)+Y(g) ![]() 3M(g)+N(s) △H<0。
3M(g)+N(s) △H<0。
部分实验数据如下:
t/s | 0 | 500 | 1000 | 1500 |
n(X)/mol | 4.00 | 2.80 | 2.00 | 2.00 |
(2)当反应达到平衡后,其他条件不变,分离出部分M,则新平衡时,正反应速率相对于原平衡____________(填“增大”、“减小”、或“不变”)。
(3)该反应达到平衡时某物理量随温度变化如下图所示。纵坐标可以表示的物理量有哪些____。

a.Y的逆反应速率
b.M的体积分数
c.混合气体的密度
d.X的转化率
(4)反应达到平衡后,若再加入3.00molM,3.00molN,下列说法正确的是_____________。
A.重新达平衡后,用X表示的υ(正)比原平衡大
B.重新达平衡后,M的体积分数小于50%
C.重新达平衡后,M的物质的量浓度是原平衡的1.5倍
D.重新达平衡后,Y的平均反应速率与原平衡相等
(5)若容器为绝热恒容容器,起始时加入4.00molX,2.00molY,则达平衡后M的物质的量浓度____________1.5mol/L(填“大于”、“小于”或“等于”)。
【题目】工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、SO2等气体,严重污染空气。对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
I. 脱硝:
已知:H2的燃烧热为285.8kJ·mol1
N2(g)+2O2(g)=2NO2(g) ΔH=+133kJ·mol1
H2O(g)=H2O(l) ΔH=44kJ·mol1
催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为:______。
II. 脱碳:
(1)向2L密闭容器中加入2mol CO2和6mol H2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g)![]() CH3OH(l)+H2O(l)
CH3OH(l)+H2O(l)
① 该反应自发进行的条件是_____(填“低温”、“高温”或“任意温度”)
② 下列叙述能说明此反应达到平衡状态的是_____。(填字母)
a. 混合气体的平均式量保持不变 b. CO2和H2的体积分数保持不变 c. CO2和H2的转化率相等
d. 混合气体的密度保持不变 e. 1 mol CO2生成的同时有3 mol HH键断裂
(2) 改变温度,使反应CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH<0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见表:
CH3OH(g)+H2O(g) ΔH<0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见表:
反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
反应I:恒温恒容 | 0min | 2 | 6 | 0 | 0 |
10min | 4.5 | ||||
20min | 1 | ||||
30min | 1 | ||||
反应II:绝热恒容 | 0min | 0 | 0 | 2 | 2 |
①达到平衡时,反应I、II对比:平衡常数K(I)___K(II)(填“>”“<”或“=”下同);平衡时CH3OH的浓度c(I)___c(II)。
②对反应I,前10min内的平均反应速率v(CH3OH)=_____。在其他条件不变的情况下,若30 min时只改变温度T2℃,此时H2的物质的量为3.2 mol,则T1____T2(填“>”、“<”或“=”)。若30 min时只向容器中再充入1 mol CO2(g)和1 mol H2O(g),则平衡_____移动(填“正向”、“逆向”或“不”)。