题目内容
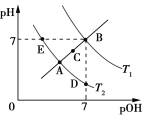
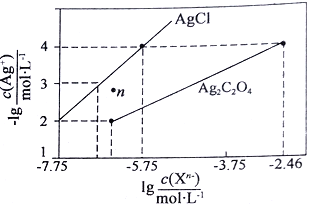
【题目】常温下,用AgNO3溶液分别滴定浓度均为0.01mol/L的KCl、K2C2O4溶液,所得的沉淀溶解平衡图象如下图所示(不考虑C2O42-的水解)。下列叙述正确的是
A.Ksp(Ag2C2O4)的数量级等于10-7
B.n点表示AgCl的不饱和溶液
C.向c(Cl-)=c(C2O42-)的混合液中滴入AgNO3溶液时,先生成Ag2C2O4 沉淀
D.Ag2C2O4+2C1-=2AgCl+C2O42-的平衡常数为109.04
【答案】D
【解析】
由图形分别求出Ag2C2O4和AgCl的Ksp,利用相关数据进行解题。
A.从图像看出,当c(C2O42-)=10-2.46 mol/L, c(Ag+)=10-4mol/L,Ksp (Ag2C2O4)= 10-2.46×(10-4)2=10-10.46,A错误;
B.根据图像可知c(Ag+)=10-4mol/L,c(Cl-)=10-5.75 mol/L,所以Ksp(AgCl)= 10-4×10-5.75=10-9.75,n点中,c(Ag+)大于平衡时的浓度,Qc(AgCl)> Ksp(AgCl),n点表示AgCl的过饱和溶液,B错误;
C.AgCl中c(Ag+)= Ksp(AgCl)/c(Cl-)=10-9.75/ c(Cl-), Ag2C2O4中
![]() ,假设c(Cl-)=c(C2O42-)=1mol,则Ag2C2O4中c(Ag+)较大,所以向c(Cl-)=c(C2O42-)的混合液中滴入AgNO3溶液时,先生成AgCl沉淀,C错误;
,假设c(Cl-)=c(C2O42-)=1mol,则Ag2C2O4中c(Ag+)较大,所以向c(Cl-)=c(C2O42-)的混合液中滴入AgNO3溶液时,先生成AgCl沉淀,C错误;
D.Ag2C2O4+2C1-=2AgCl+C2O42-的平衡常数为c(C2O42-)/ c2(Cl-)= c(C2O42-)×c2(Ag+)/ c2(Cl-)×c2(Ag+)=10-10.46/(10-9.75)2=109.04,D正确。
答案选D。

 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案