��Ŀ����
��ԴΣ����ʹ�������Ѱ���µ������Դ�Ϳ�չ��������Դ����Ч���á��ļ����з������ȼ�ϵ��ʹ��������ֱ�Ӳ��������DZ����������ս�ԵĿ���֮һ���Զ��飨��֪�����ȼ����Ϊ2 877.6 kJ��mol��1��Ϊ�����ش��������⣺
��1��д������ȼ�յ��Ȼ�ѧ����ʽ��________________��
��2���������ȼ���ȣ�2 878 kJ��mol��1���춡���ȼ���ȣ�2 869 kJ��mol����������ת��Ϊ�춡��Ĺ�����________����ų��������ա���������
��1��2C4H10��g����13O2��g��=8CO2��g����10H2O��l������H����5 755.2 kJ��mol��1
��2���ų�
����

�״�ȼ�Ϸ�Ϊ�״����ͺͼ״����͡���ҵ�Ϻϳɼ״��ķ����ܶࡣ
��1��һ�������·�����Ӧ��
CO2(g) +3H2(g) ��CH3OH(g)+H2O(g) ��H1
2CO (g) +O2(g) ��2CO2(g) ��H2
2H2(g)+O2(g) ��2H2O(g) ��H3
��CO(g) + 2H2(g)  CH3OH(g)���ġ�H�� ��
CH3OH(g)���ġ�H�� ��
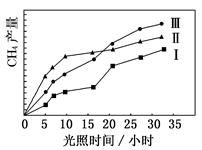
��2�����ݻ�Ϊ2L���ܱ������н��з�Ӧ��CO(g)+2H2(g) CH3OH(g) �������������䣬��300���500��ʱ�����ʵ���n(CH3OH) �뷴Ӧʱ��t�ı仯������ͼ��ʾ���÷�Ӧ�ġ�H 0 ����>��<��=����
CH3OH(g) �������������䣬��300���500��ʱ�����ʵ���n(CH3OH) �뷴Ӧʱ��t�ı仯������ͼ��ʾ���÷�Ӧ�ġ�H 0 ����>��<��=����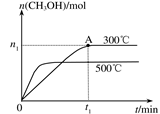
��3����Ҫ��״��IJ��ʣ��ɲ�ȡ�Ĵ�ʩ��____________������ĸ����
| A����������� |
| B�������¶� |
| C�������¶� |
| D��ʹ�ú��ʵĴ��� |
��4��CH4��H2O�ڴ������淢����ӦCH4+H2O
 CO+3H2��T��ʱ����1 L�ܱ�������Ͷ��1 mol CH4��1 mol H2O(g)��5Сʱ���÷�Ӧ��ϵ�ﵽƽ��״̬����ʱCH4��ת����Ϊ50% ��������¶��µ�ƽ�ⳣ�� ���������С�������λ���֣���
CO+3H2��T��ʱ����1 L�ܱ�������Ͷ��1 mol CH4��1 mol H2O(g)��5Сʱ���÷�Ӧ��ϵ�ﵽƽ��״̬����ʱCH4��ת����Ϊ50% ��������¶��µ�ƽ�ⳣ�� ���������С�������λ���֣�����5���Լ״�Ϊȼ�ϵ����͵�أ���ɱ�����������Ϊȼ�ϵ� ��ͳȼ�ϵ�أ�Ŀǰ�õ��㷺���о�����ͼ��Ŀǰ�о��϶��һ�����������ȼ�ϵ�ع���ԭ��ʾ��ͼ���ش��������⣺

��B���ĵ缫��ӦʽΪ ��
�����ø�ȼ�ϵ������Դ����ʯī���缫�������ͭ��Һ������·��ת��1mole- ʱ��ʵ�������ĵļ״��������������ϴ���ԭ���� ��
��6��25��ʱ������Ƶ�Ksp=4.0��10-8,̼��Ƶ�Ksp=2.5��10-9����20ml̼��Ƶı�����Һ����μ���8.0��10-4 mol��L-1�IJ������Һ20ml���ܷ�������� ����ܡ�����
���ڹ�����ռ����Ҫ��λ��
��1���ϳɰ���ҵ�У��ϳ�����ÿ����2 mol NH3���ų�92.2 kJ������
�� ��ҵ�ϳɰ����Ȼ�ѧ����ʽ�� ��
�� ����ʼʱ�������ڷ���2 mol N2��6 mol H2����ƽ���ų�������ΪQ����
Q���>������<����=����_______184.4 kJ��
�� ��֪��
1 mol N-H���������յ�����Լ����_______kJ��
��2����ҵ�������ص�ԭ������NH3��CO2Ϊԭ�Ϻϳ�����[CO(NH2)2]����Ӧ�Ļ�ѧ����ʽΪ��2NH3 (g)+ CO2 (g)  CO(NH2)2 (l) + H2O (l)���÷�Ӧ��ƽ�ⳣ�����¶ȹ�ϵ���£�
CO(NH2)2 (l) + H2O (l)���÷�Ӧ��ƽ�ⳣ�����¶ȹ�ϵ���£�
| T / �� | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
���ʱ䦤H���>������<����=���� 0
����һ���¶Ⱥ�ѹǿ�£���ԭ�����е�NH3��CO2������ ����֮�ȣ���̼�ȣ�
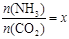 ����ͼ�ǰ�̼�ȣ�x����CO2ƽ��ת���ʣ������Ĺ�ϵ��������x����������ԭ���� ��
����ͼ�ǰ�̼�ȣ�x����CO2ƽ��ת���ʣ������Ĺ�ϵ��������x����������ԭ���� ��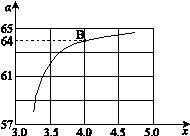
�� ��ͼ�е�B�㴦��NH3��ƽ��ת����Ϊ_______��
��3���������Ʊ������������һ����Ҫ���ʣ������Ļ�������;�㷺��
���������õ����Ʊ������������һ��;����

�ٹ��̢�Ļ�ѧ����ʽ��
������ʱ���Ͻ�NH3��±�أ���Cl2����װ���䡣�����߽Ӵ�ʱ���ҷ�Ӧ�������̣�����0.4 mol NH3�μӷ�Ӧʱ��0.3 mol ����ת�ơ�д����Ӧ�Ļ�ѧ����ʽ
�۰���һ��DZ�ڵ������Դ������������ȼ�ϵ�ص�ȼ�ϡ�
��֪��4NH3(g) + 3O2(g) = 2N2(g) + 6H2O(g) ��H =" �D1316" kJ/mol�����ȼ�ϵ�صĸ�����Ӧʽ�� ��
X��Y��Z��W��Ϊ10���ӵķ��ӻ����ӡ�X��5��ԭ�Ӻˡ�ͨ��״���£�WΪ��ɫҺ�塣����֮��ת����ϵ��ͼ��ʾ����ش�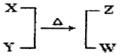
��1����ҵ��ÿ��ȡ1molZҪ�ų�46.2 kJ��������д���÷�Ӧ���Ȼ�ѧ����ʽ�� ��
��2����ҵ��ȡZ�Ļ�ѧƽ�ⳣ��K��T�Ĺ�ϵ���±���
| T/K | 298 | 398 | 498 | ���� |
| K/(mol��L��1)��2 | 4.1��106 | K1 | K2 | ���� |
������������⣺
���ԱȽ�K1��K2�Ĵ�С��K1 K2����д��>����=����<����
�ں��¹̶�����������У����и�������Ϊ�жϸ÷�Ӧ�ﵽ��ѧƽ��״̬�����ݵ��� ���������ĸ����
A�������ڸ����ʵ�Ũ��֮��Ϊ��ѧ��������
B����������ܶȱ��ֲ���
C��������ѹǿ���ֲ���
D�����������Է����������ֲ���
��3��ij��ѧС��ͬѧģ�ҵ������ȡHNO3�������ͼ��ʾװ�ã�����aΪһ���ɳ��������������Ƥ��
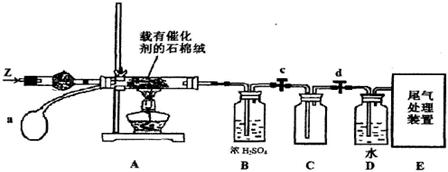
��A�з�����Ӧ�Ļ�ѧ����ʽ�� ��
��B��ŨH2SO4�������� ��
��4��д��Dװ���з�Ӧ�Ļ�ѧ����ʽ ��
��5��a��ͨ����������� ��
 CO(g)��3H2(g)���÷�Ӧ��H����206 kJ��mol��1��
CO(g)��3H2(g)���÷�Ӧ��H����206 kJ��mol��1�� CO(g)��H2(g)��C(s)��CO(g)��H2(g)��ȫȼ�յ��Ȼ�ѧ����ʽΪ��
CO(g)��H2(g)��C(s)��CO(g)��H2(g)��ȫȼ�յ��Ȼ�ѧ����ʽΪ��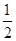 O2(g)=H2O(g)����H����242.0 kJ��mol��1
O2(g)=H2O(g)����H����242.0 kJ��mol��1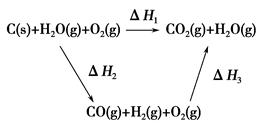
 CH3OH(g) +H2O(g) ��H
CH3OH(g) +H2O(g) ��H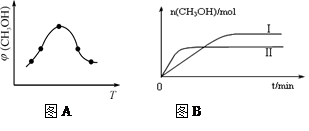
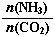 ��3����ƽ��ʱCO2��ת����Ϊ60%����NH3��ƽ��ת����Ϊ ��
��3����ƽ��ʱCO2��ת����Ϊ60%����NH3��ƽ��ת����Ϊ �� H2(g)��CO2(g)����H2��
H2(g)��CO2(g)����H2��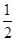 O2(g)=FeO(s)����H����272.0 kJ��mol��1
O2(g)=FeO(s)����H����272.0 kJ��mol��1 O2(g)=Al2O3(s)����H����1675.7 kJ��mol��1
O2(g)=Al2O3(s)����H����1675.7 kJ��mol��1
 Na2S(s)��4H2O(g)
Na2S(s)��4H2O(g)