题目内容
【题目】欲用98%的浓硫酸(ρ=1.84g·cm-3)配制成浓度为0.5mol·L-1的稀硫酸480ml。
若实验仪器有: A.10 mL量筒 B.20 mL量筒 C.托盘天平 D.玻璃棒
E.100 mL容量瓶 F.250 mL容量瓶 G.500 mL容量瓶 H.胶头滴管 I.200 mL烧杯
(1)所需浓硫酸的体积为______mL(保留到小数点后一位)。
(2)实验时需选用的仪器有D、I、 ______________________(填序号)。
(3)请将下列各操作,按正确的序号填在横线上(可重复使用)。
A.用量筒量取浓H2SO4;B.反复颠倒摇匀;C.用胶头滴管加蒸馏水至刻度线
D.洗净所用仪器;E.稀释浓H2SO4;F.将溶液转入容量瓶
其操作正确的顺序依次为____________________________。
(4) 配制过程中,下列操作会使配制的稀硫酸溶液浓度偏高的是(填序号)________。
①量取浓硫酸的量筒用蒸馏水洗涤2~3次,并把洗涤液转入容量瓶
②容量瓶使用时未干燥
③定容时俯视读数
④定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
【答案】 13.6 B、G、H D、A、E、F、D、C、B ①、③
【解析】(1)浓硫酸的浓度是![]() ,需要使用500mL容量瓶,则所需浓硫酸的体积为
,需要使用500mL容量瓶,则所需浓硫酸的体积为![]() 。(2)实验时需选用的仪器有20mL量筒、烧杯、玻璃棒、500mL容量瓶和胶头滴管,即为D、I、B、G、H;(3)操作的一般过程是计算、量取、稀释、冷却、转移、洗涤、振荡、定容、摇匀等,因此操作正确的顺序依次为D、A、E、F、D、C、B;(4)①量取浓硫酸的量筒用蒸馏水洗涤2~3次,并把洗涤液转入容量瓶中,溶质的物质的量增加,浓度偏高;②容量瓶使用时未干燥不影响;③定容时俯视读数,溶液体积减少,浓度偏高;④定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线,溶液体积增加,浓度偏低,答案选①③。
。(2)实验时需选用的仪器有20mL量筒、烧杯、玻璃棒、500mL容量瓶和胶头滴管,即为D、I、B、G、H;(3)操作的一般过程是计算、量取、稀释、冷却、转移、洗涤、振荡、定容、摇匀等,因此操作正确的顺序依次为D、A、E、F、D、C、B;(4)①量取浓硫酸的量筒用蒸馏水洗涤2~3次,并把洗涤液转入容量瓶中,溶质的物质的量增加,浓度偏高;②容量瓶使用时未干燥不影响;③定容时俯视读数,溶液体积减少,浓度偏高;④定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线,溶液体积增加,浓度偏低,答案选①③。

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案【题目】如表为元素周期表的一部分.
碳 | 氮 | Y | |
X | 硫 | Z |
回答下列问题:
(1)Z元素在周期表中的位置为 .
(2)表中元素原子半径最大的是(填元素符号) .
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是 . a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)沸点:H2YH2S(填“>”或“=”或“<”),理由是 .
(5)Y2和Y3互为(填“同位素”或“同分异构体”或“同素异形体”).
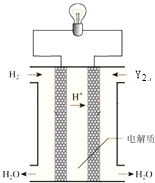
(6)其中单质Y2可用做如图所示装置(燃料电池)的氧化剂,请写出Y2在酸性电解质溶液中发生的电极反应方程式 .