题目内容
1.在恒温下的密闭容器中,有可逆反应:2NO(g)+O2(g)?2NO2(g)(反应放热),能说明已达到平衡状态的是( )| A. | 正反应生成NO2的速率和逆反应生成O2的速率相等 | |
| B. | N2O4和NO2的浓度相等 | |
| C. | 混合气体的颜色保持不变 | |
| D. | 单位时间内生成1mol O2的同时,生成1molNO |
分析 A、正反应生成NO2的速率和逆反应生成O2的速率等于2:1时,反应达到平衡状态.
B、平衡时各物质浓度大小决定于开始加入的多少和反应程度;
C、混合气体的颜色不再改变,说明NO2气体的浓度不变;
D、生成氧气和生成NO都是逆反应,不能说明正逆反应速率相等.
解答 解:A、正反应生成NO2的速率和逆反应生成O2的速率等于2:1时,反应达到平衡状态,故A错误;
B、平衡时各物质浓度大小决定于开始加入的多少和反应程度,N2O4和NO2的浓度相等,不能说明反应达到平衡状态,故B错误;
C、混合气体的颜色不再改变,说明NO2气体的浓度不变,达到平衡状态,故C正确;
D、生成氧气和生成NO都是逆反应,不能说明正逆反应速率相等,故D错误;
故选C.
点评 本题考查化学平衡状态的判断,题目难度不大,做题时注意分析化学方程式的前后计量数大小的关系.

练习册系列答案
相关题目
11.下列离子方程式的书写正确的是( )
| A. | 0.1 mol•L-1的NaHSO3溶液与0.2 mol•L-1的NaClO溶液等体积混合:HSO3-+ClO-=SO42-+Cl-+H+ | |
| B. | 等浓度的Fe2(SO4)3溶液和Ba(OH)2溶液混合:2Fe3++3SO42-+3Ba2++6OH-=2Fe(OH)3↓+3BaSO4↓ | |
| C. | Ca(HCO3)2溶液与少量NaOH溶液反应:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O | |
| D. | H218O中投入过氧化钠:2H218O+2Na2O2=4Na++4OH-+18O2↑ |
12.如图是氢氧燃料电池(电解质为KOH)构造示意图.关于该电池的说法不正确的是( )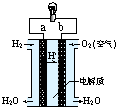

| A. | 电子由b通过灯泡流向a | |
| B. | 氢氧燃料电池是环保电池 | |
| C. | a极是负极 | |
| D. | 正极的电极反应是:O2+2H2O+4e-=4OH- |
9.下列一定能说明HNO2是弱电解质的是( )
①相同条件下,同浓度的HNO2的导电性比盐酸弱 ②用HNO2作导电实验,灯泡很暗
③HNO2能使石蕊试液变红 ④0.1mol/L HNO2溶液的c(H+)=10-2mol/L.
①相同条件下,同浓度的HNO2的导电性比盐酸弱 ②用HNO2作导电实验,灯泡很暗
③HNO2能使石蕊试液变红 ④0.1mol/L HNO2溶液的c(H+)=10-2mol/L.
| A. | ①②③ | B. | ②③④ | C. | ①④ | D. | ②④ |
10.用NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 用含0.1mol FeCl3的溶液与足量沸水反应制得的Fe(OH)3胶体中胶粒数为0.1NA | |
| B. | 0.1mol Fe 与0.1mol Cl2充分反应,转移的电子数为0.3 NA | |
| C. | 46g NO2和N2O4的混合气体中含N原子总数为NA | |
| D. | 等物质的量的NH4+和OH-含电子数均为10NA |
11.在2L密闭容器中加入4molA和6molB,发生以下反应:4A(g)+6B(g)?4C(g)+5D(g).若经5s后,剩下的A是2.5mol,则A的反应速率是( )
| A. | 0.45 mol/(L•s) | B. | 0.15 mol/(L•s) | C. | 0.225 mol/(L•s) | D. | 0.9 mol/(L•s) |
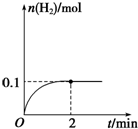 一定温度下,向1L密闭容器中加入1mol HI(g),发生反应2HI?H2+I2,H2物质的量随时间的变化如图所示.
一定温度下,向1L密闭容器中加入1mol HI(g),发生反应2HI?H2+I2,H2物质的量随时间的变化如图所示.
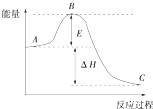 2SO2(g)+O2(g)═2SO3(g)反应过程的能量变化如图所示,已知1mol SO2(g) 被氧化为1mol SO3(g)的△H=-99kJ/mol.回答下列问题:
2SO2(g)+O2(g)═2SO3(g)反应过程的能量变化如图所示,已知1mol SO2(g) 被氧化为1mol SO3(g)的△H=-99kJ/mol.回答下列问题: