题目内容
9.某烃的分子式为C11H20,1mol该烃在催化剂作用下可以吸收2molH2,用热的酸性KMnO4溶液氧化,得到下列两种有机物:CH3COOH、CH3CO CH2CH2CH2CH2COCH3.由此推断该烃可能的结构简式是( )| A. |  | B. |  | ||
| C. |  | D. | 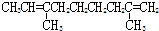 |
分析 某烃的分子式为C11H20,该烃的不饱和度=$\frac{11×2+2-20}{2}$=2,1mol该烃在催化剂作用下可以吸收2molH2,说明该分子中含有2个碳碳双键或1个碳碳三键,用热的酸性KMnO4溶液氧化,得到下列两种有机物:CH3COOH、CH3COCH2CH2CH2CH2COCH3,不饱和烃被酸性高锰酸钾溶液氧化时,碳碳双键被氧化,生成羧基或羰基,据此判断该烃可能结构简式.
解答 解:某烃的分子式为C11H20,该烃的不饱和度=$\frac{11×2+2-20}{2}$=2,1mol该烃在催化剂作用下可以吸收2molH2,说明该分子中含有2个碳碳双键或1个碳碳三键,不饱和烃被酸性高锰酸钾溶液氧化时,碳碳双键被氧化,生成羧基或羰基,用热的酸性KMnO4溶液氧化,得到下列两种有机物:CH3COOH、CH3COCH2CH2CH2CH2COCH3,则该烃结构简式可能是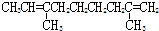 ,故选D.
,故选D.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,利用逆向思维分析判断即可,题目难度不大.

练习册系列答案
相关题目
20.设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
| A. | 标准状况下,22.4LNO与CO2的混合气体中含有O原子数为3NA | |
| B. | 0.1mol NH3溶于足量水中(不考虑氨气挥发),溶液中N原子的数目为0.1NA | |
| C. | 0.1molN2与足量的H2反应,转移的电子数是0.6NA | |
| D. | 58.5 g的NaCl固体中含有NA个氯化钠分子 |
17.对于合成氨反应N2(g)+3H2(g)?2NH3(g)△H=-92kJ/mol,下列说法正确的是( )
| A. | 若起始加入2molN2和6molH2发生反应,则平衡时N2和H2的转化率相同 | |
| B. | 该反应采用高温条件,有利于提高NH3的产率,从而提高生产效率 | |
| C. | 若起始加入2molN2和6molH2发生反应,平衡时测得反应共放热46kJ,则N2的平衡转化率为50% | |
| D. | 若平衡时保持其它条件不变,压缩容器体积,则平衡正向移动,N2的浓度减小,NH3的浓度增大 |
4.下列表示对应化学反应的离子方程式正确的是( )
| A. | Na2O2溶于水产生O2:Na2O2+H2O═2Na++2OH-+O2↑ | |
| B. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O | |
| C. | 向FeBr2溶液中通入足量 Cl2:2Fe2++2Br-+2Cl2═Br2+2Fe3++4Cl- | |
| D. | 向50 mL 1 mol•L-1明矾溶液中滴入两滴0.1 mol•L-1Ba(OH)2溶液:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ |
18.下列溶液中,溶质的物质的量浓度为1mol•L-1的是( )
| A. | 将40gNaOH溶于1L水所得的溶液 | |
| B. | 将22.4LHCl溶于水配成1L溶液 | |
| C. | 1L含2mol K+的K2SO4溶液 | |
| D. | 将0.5mol•L-1的NaNO3溶液100mL加热蒸发掉50g水后的溶液 |
19.由C5H10、C2H4O2、C3H6O2和C6H12O6组成的混合物,经测定含氧元素的质量分数为x,则此混合物中含碳元素的质量分数为( )
| A. | $\frac{6(1-x)}{7}$ | B. | $\frac{1-x}{7}$ | C. | $\frac{3x}{4}$ | D. | 无法计算 |
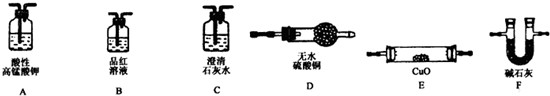
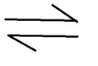 Fe3++3OH-.
Fe3++3OH-.