题目内容
17.如图是CO2电催化还原为CH4的工作原理示意图.下列说法不正确的是( )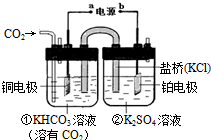
| A. | 该过程是电能转化为化学能的过程 | |
| B. | 铜电极的电极反应式为CO2+8H++8e-=CH4+2H2O | |
| C. | 一段时间后,②池中溶液的pH一定增大 | |
| D. | 盐桥中K+移向铜电极 |
分析 CO2电催化还原为CH4,则通入CO2的一极为电解池的阴极,电极方程式为CO2+8H++8e-═CH4+2H2O,则a为负极,b为正极,阳极发生氧化反应,生成氧气,以此解答该题.
解答 解:A.该装置是一个电解池,电解池是将电能转化为化学能的装置,故A正确;
B.CO2电催化还原为CH4的过程是一个还原反应过程,所以铜电解是电解池的阴极,铜电极的电极反应式为CO2+8H++8e-═CH4+2H2O,故B正确;
C.在电解池的阳极上,是阴离子氢氧根离子发生失电子的氧化反应,所以酸性增强,pH一定下降,故C错误;
D.阳离子向阴极移动,所以K+移向铜电极,故D正确;
故选C.
点评 本题考查学生电解池的工作原理知识,为高频考点,侧重于学生的分析能力的考查,注意两极反应式的书写以及氧化还原反应之间的关系,注意规律的总结是关键,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.下列装置能达到对应实验目的是( )
| A. |  分离碘与沙子 | B. | 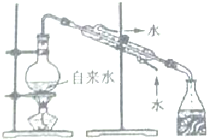 实验室制取蒸馏水 | ||
| C. | 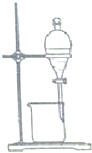 乙醇提取碘水中的碘 | D. | 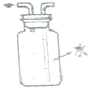 收集氨气 |
11.X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示.Z为地壳中含量最多的金属元素,下列说法中正确的是( )
| X | Y | |||
| Z | W | Q |
| A. | X、Y、W三种元素最低价氢化物的沸点依次升高 | |
| B. | 原子半径:Q>W>Z>Y>X | |
| C. | 最高价氧化物对应水化物的酸性:Q>W>Z | |
| D. | X及Q的气态氢化物相反应,形成的化合物为离子化合物 |
7.常温下,在下列指定条件的各溶液中,一定能大量共存的离子组是( )
| A. | 含0.1 molL-1SO2的溶液中:Na+、Ba2+、Br-、Cl- | |
| B. | 能与金属铝反应放出氢气的溶液中:K+、Mg2+、NO${\;}_{3}^{-}$、SiO${\;}_{3}^{2-}$ | |
| C. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=10-12的溶液中:K+、NH${\;}_{4}^{+}$、SO${\;}_{4}^{2-}$、NO${\;}_{3}^{-}$ | |
| D. | 不能使酚酞变红的无色溶液中:Na+、K+、ClO-、I- |
12.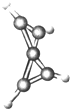 科学家最近在-100℃的低温下合成了一种烃X,红外光谱和核磁共振表明其分子中氢原子的化学环境没有区别,根据分析,绘制了分子的球棍模型,如图,下列说法中不正确的是( )
科学家最近在-100℃的低温下合成了一种烃X,红外光谱和核磁共振表明其分子中氢原子的化学环境没有区别,根据分析,绘制了分子的球棍模型,如图,下列说法中不正确的是( )
 科学家最近在-100℃的低温下合成了一种烃X,红外光谱和核磁共振表明其分子中氢原子的化学环境没有区别,根据分析,绘制了分子的球棍模型,如图,下列说法中不正确的是( )
科学家最近在-100℃的低温下合成了一种烃X,红外光谱和核磁共振表明其分子中氢原子的化学环境没有区别,根据分析,绘制了分子的球棍模型,如图,下列说法中不正确的是( )| A. | 该烃X与等质量的甲烷相比,X燃烧时消耗的氧气更多 | |
| B. | 分子中碳原子的化学环境有2种 | |
| C. | 分子中的氢原子分布在两个互相垂直的直线上 | |
| D. | 分子中有C-C键,也有C=C键 |
6.下列说法或表示方法正确的是( )
| A. | 凡是吸热或放热过程中热量的变化均称为反应热 | |
| B. | 热化学方程式中的化学计量数只表示物质的量,可以是分数 | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷燃烧热 |