题目内容
6.下列说法或表示方法正确的是( )| A. | 凡是吸热或放热过程中热量的变化均称为反应热 | |
| B. | 热化学方程式中的化学计量数只表示物质的量,可以是分数 | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷燃烧热 |
分析 A.如没有发生化学变化,则不是反应热;
B.热化学方程式中的化学计量数只表示物质的量,不表示分子数;
C.反应是否加热与反应热无关;
D.根据燃烧热的定义判断.
解答 解:A.反应热为化学反应中的能量变化,物理变化中的能量变化不能称为反应热,如聚集状态的改变,故A错误;
B.热化学方程式中的化学计量数只表示物质的量,不表示分子数,所以可用分数或小数表示,故B正确;
C.需要加热才能发生的反应不一定为吸热反应,如铝热反应需要在高温条件下才能进行,但为放热反应,故C错误;
D.1mol可燃物燃烧生成稳定氧化物放出的热量是燃烧热,而1mol甲烷燃烧生成气态水不是稳定氧化物,应为液态水和二氧化碳所放出的热量是甲烷的燃烧热,故D错误;
故选B.
点评 本题考查较综合,为高频考点,涉及反应中能量变化及燃烧热等,侧重高考高频考点的考查,注意AC利用实例分析,题目难度不大.

练习册系列答案
相关题目
19. 短周期元素X、Y、Z、W在周期表中的相对位置如图,X的气态氢化物能与其最高价氧化物对应的水化物反应生成盐.下列判断错误的是( )
短周期元素X、Y、Z、W在周期表中的相对位置如图,X的气态氢化物能与其最高价氧化物对应的水化物反应生成盐.下列判断错误的是( )
 短周期元素X、Y、Z、W在周期表中的相对位置如图,X的气态氢化物能与其最高价氧化物对应的水化物反应生成盐.下列判断错误的是( )
短周期元素X、Y、Z、W在周期表中的相对位置如图,X的气态氢化物能与其最高价氧化物对应的水化物反应生成盐.下列判断错误的是( )| A. | 最简单气态氢化物的稳定性:X>Y | |
| B. | 单核阴离子半径:Z>W | |
| C. | 含Z元素的盐溶液可能显酸性、碱性或中性 | |
| D. | W元素的单质具有漂白性,常用于自来水的杀菌消毒 |
17.如图是CO2电催化还原为CH4的工作原理示意图.下列说法不正确的是( )
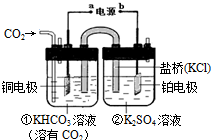

| A. | 该过程是电能转化为化学能的过程 | |
| B. | 铜电极的电极反应式为CO2+8H++8e-=CH4+2H2O | |
| C. | 一段时间后,②池中溶液的pH一定增大 | |
| D. | 盐桥中K+移向铜电极 |
1.某高分子化合物(C13H16)n,它是由单体A与苯乙烯( )共聚而成,则单体A可能为( )
)共聚而成,则单体A可能为( )
 )共聚而成,则单体A可能为( )
)共聚而成,则单体A可能为( )| A. | C2H5-CH═CH-CH3 | B. |  | C. |  | D. | CH3C═CH-CH2CH3 |
11.只用水就能鉴别出的一组物质是( )
| A. | 苯、乙酸、乙醇 | B. | 乙醇、乙醛、乙酸 | ||
| C. | 苯、乙酸、四氯化碳 | D. | 硝基苯、四氯化碳、乙醇 |
 2H2(g)+S2(g)△H
2H2(g)+S2(g)△H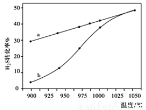
 应制取H2,反应方程式如下:
应制取H2,反应方程式如下: