题目内容
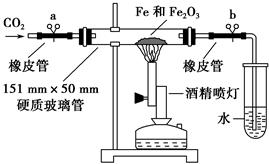
实验题(14分):Ⅰ、HCOOH是一种无色、易挥发的液体,某学习小组参照: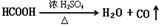 原理,用下列仪器(加热及固定装置省略)制备干燥、纯净的CO,并用CO还原CuO粉末。
原理,用下列仪器(加热及固定装置省略)制备干燥、纯净的CO,并用CO还原CuO粉末。
(1)若所制气体流向从左向右时,上述仪器连接为: A→( ) →( )→( )→( ) →( )
(2)A装置中小试管的作用(至少答两条):
① 。② 。
(3)证明HCOOH受热产物中有CO的现象为: 。
(4)本实验有3处用到酒精灯,除A、B处外,还缺一个酒精灯,应放在 处.
Ⅱ、学习小组查阅资料知:
Cu的颜色为红色或紫红色,而Cu2O的颜色也为红色或砖红色。②4CuO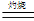 2 Cu2O + O2↑;③ Cu2O +2H+
2 Cu2O + O2↑;③ Cu2O +2H+
= Cu+Cu2+ + H2O ;因此对CO充分还原CuO后所得红色固体是否含有Cu2O进行了认真的研究,提出下列设计方案:
方案①:取该红色固体溶于足量稀硝酸中,观察溶液颜色的变化。
方案②:取该红色固体溶于足量稀硫酸中,观察溶液颜色的变化。
(5)写出Cu2O与稀硝酸反应的化学方程式: 。
(6)请你评价方案②的合理性,并简述理由:方案②: ,理由: 。
 原理,用下列仪器(加热及固定装置省略)制备干燥、纯净的CO,并用CO还原CuO粉末。
原理,用下列仪器(加热及固定装置省略)制备干燥、纯净的CO,并用CO还原CuO粉末。
(1)若所制气体流向从左向右时,上述仪器连接为: A→( ) →( )→( )→( ) →( )
(2)A装置中小试管的作用(至少答两条):
① 。② 。
(3)证明HCOOH受热产物中有CO的现象为: 。
(4)本实验有3处用到酒精灯,除A、B处外,还缺一个酒精灯,应放在 处.
Ⅱ、学习小组查阅资料知:
Cu的颜色为红色或紫红色,而Cu2O的颜色也为红色或砖红色。②4CuO
 2 Cu2O + O2↑;③ Cu2O +2H+
2 Cu2O + O2↑;③ Cu2O +2H+= Cu+Cu2+ + H2O ;因此对CO充分还原CuO后所得红色固体是否含有Cu2O进行了认真的研究,提出下列设计方案:
方案①:取该红色固体溶于足量稀硝酸中,观察溶液颜色的变化。
方案②:取该红色固体溶于足量稀硫酸中,观察溶液颜色的变化。
(5)写出Cu2O与稀硝酸反应的化学方程式: 。
(6)请你评价方案②的合理性,并简述理由:方案②: ,理由: 。
(1)、A→(F ) →(C )→( E )→( B ) →( D )
(2)、①液封,防止气体从长颈漏斗中溢出 ②节约试剂 ③便于控制反应
(3)、B中黑色固体变为红色,D中溶液变浑浊。
(4)、g(或D) (5)、3Cu2O +14HNO3=6Cu(NO3)2+2NO↑ + 7H2O
(6)、合理 因为Cu2O可与稀硫酸溶液反应生成Cu2+ ,会使溶液变蓝。
(2)、①液封,防止气体从长颈漏斗中溢出 ②节约试剂 ③便于控制反应
(3)、B中黑色固体变为红色,D中溶液变浑浊。
(4)、g(或D) (5)、3Cu2O +14HNO3=6Cu(NO3)2+2NO↑ + 7H2O
(6)、合理 因为Cu2O可与稀硫酸溶液反应生成Cu2+ ,会使溶液变蓝。
试题分析:(1)用仪器组装设备的顺序是制取气体的装置、然后除杂、干燥装置、检验装置、反应装置、检验装置、尾气处理装置。有时为了安全起见,要加一个安全瓶,来防止倒吸现象的发生。因此若所制气体流向从左向右时。装置的连接顺序是A→F→C→E→B→D;(2)A装置中小试管的作用①液封,防止气体从长颈漏斗中溢出;②节约试剂;③便于控制反应;(3)若有CO气体产生,则在B中会发生反应:CuO+CO
 CO2+Cu,Cu是红色固体,CO2能使澄清的石灰水变浑浊。因此要证明HCOOH受热产物中有CO的现象为B中黑色固体变为红色,D中溶液变浑浊。(4)本实验有3处用到酒精灯,在A用于制取CO气体,在B处用于使CO与CuO发生氧化还原反应,在D处用于除去过量的CO,防止污染大气。(5)Cu2O与稀硝酸发生氧化还原反应的化学方程式是3Cu2O +14HNO3=6Cu(NO3)2+2NO↑ + 7H2O;(6)若固体是Cu单质,与稀硫酸不反应,若固体含有Cu2O,加入稀硫酸会发生反应:Cu2O +2H+ = Cu+Cu2+ + H2O,会产生Cu2+ ,使溶液变蓝。因此方案②合理。
CO2+Cu,Cu是红色固体,CO2能使澄清的石灰水变浑浊。因此要证明HCOOH受热产物中有CO的现象为B中黑色固体变为红色,D中溶液变浑浊。(4)本实验有3处用到酒精灯,在A用于制取CO气体,在B处用于使CO与CuO发生氧化还原反应,在D处用于除去过量的CO,防止污染大气。(5)Cu2O与稀硝酸发生氧化还原反应的化学方程式是3Cu2O +14HNO3=6Cu(NO3)2+2NO↑ + 7H2O;(6)若固体是Cu单质,与稀硫酸不反应,若固体含有Cu2O,加入稀硫酸会发生反应:Cu2O +2H+ = Cu+Cu2+ + H2O,会产生Cu2+ ,使溶液变蓝。因此方案②合理。
练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案
相关题目