题目内容
在给定条件下,氮气与氢气在密闭容器中合成氨.起始时加入氮气和氢气且浓度分别为1.0mol/L 和3.0mol/L,2秒后,氮气的浓度为0.8mol/L,氢气的浓度为2.4mol/L,氨气的浓度为0.4mol/L.分别用氮气、氢气和氨气的浓度变化表示的这2秒内的化学反应速率是多少?有什么关系:
考点:反应速率的定量表示方法
专题:化学反应速率专题
分析:根据v=
进行计算.
| △c |
| t |
解答:
解:v(N2)=
=0.1mol?L-1?s-1;
v(H2)=
=0.3mol?L-1?s-1;
v(NH3)=
=0.2mol?L-1?s-1;
v(N2):v(H2):v(NH3)=0.1:0.3:0.2=1:3:2,化学反应速率之比等化学计量数之比,
答:v(N2)=0.1mol?L-1?s-1;v(H2)=0.3mol?L-1?s-1;v(NH3)=0.2mol?L-1?s-1;化学反应速率之比等化学计量数之比.
| 1-0.8 |
| 2s |
v(H2)=
| 3-2.4 |
| 2 |
v(NH3)=
| 0.4-0 |
| 2 |
v(N2):v(H2):v(NH3)=0.1:0.3:0.2=1:3:2,化学反应速率之比等化学计量数之比,
答:v(N2)=0.1mol?L-1?s-1;v(H2)=0.3mol?L-1?s-1;v(NH3)=0.2mol?L-1?s-1;化学反应速率之比等化学计量数之比.
点评:本题考查化学反应速率的相关计算,难度不大.要注意化学反应速率之比等化学计量数之比.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
根据已知条件,对物质的性质强弱判断不正确的是( )
| A、已知HF的共价键键能比HCl大,说明稳定性:HF>HCl | ||||
| B、已知正反应的活化能大于逆反应的活化能,说明总能量:生成物>反应物 | ||||
C、已知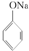 +SO2+H2O→ +SO2+H2O→ +Na2SO3,说明给出质子能力:HSO3->苯酚 +Na2SO3,说明给出质子能力:HSO3->苯酚 | ||||
D、已知CaCO3+SiO2
|
下列实验操作正确的是( )
| A、给容量瓶检漏时,向容量瓶中注入适量水,左手托住瓶底右食指顶住瓶塞,倒置数次,观察是否漏水 |
| B、具有腐蚀性的药品,必须放在玻璃器皿里称量,其他固体药品可直接放在天平托盘上称量 |
| C、配制一定物质的量浓度的溶液时,蒸馏水洗净后容量瓶未干燥,不影响测定结果 |
| D、配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸 |
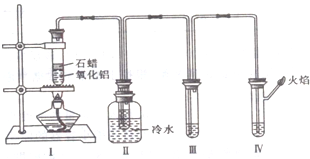
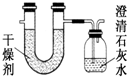 已知某种燃料含有碳、氢、氧三种元素.为了测定这种燃料中碳和氢两种元素的质量比,可将气态燃料放入足量的O2中燃烧,并将产生的气体全部通过图示装置,得到如表所列的实验数据(产生的气体完全被吸收).
已知某种燃料含有碳、氢、氧三种元素.为了测定这种燃料中碳和氢两种元素的质量比,可将气态燃料放入足量的O2中燃烧,并将产生的气体全部通过图示装置,得到如表所列的实验数据(产生的气体完全被吸收).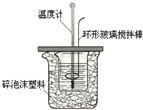 某实验小组设计用50mL 1.0mol/L盐酸跟50mL 1.1mol/L氢氧化钠溶液在如图装置中进行中和反应.在大烧杯底部垫泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:
某实验小组设计用50mL 1.0mol/L盐酸跟50mL 1.1mol/L氢氧化钠溶液在如图装置中进行中和反应.在大烧杯底部垫泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题: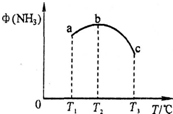 合成氨和制备硝酸是两种重要的化工生产,重庆某化工厂将合成氨与制备硝酸进行连续生产.
合成氨和制备硝酸是两种重要的化工生产,重庆某化工厂将合成氨与制备硝酸进行连续生产.