题目内容
下列图示与对应的叙述相符合的是

2N02(g) N204(g),相同时间后测得N02含量的曲线,则该反应的△H<O
N204(g),相同时间后测得N02含量的曲线,则该反应的△H<O

| A.图l为某金属单质晶体中原子的堆积方式,则其晶胞构型为体心立方 |
| B.图2为钢闸门的防腐原理示意图,则钢闸门应与电源的正极相连 |
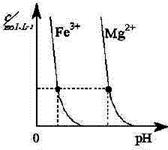
| C.图3表示CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b |
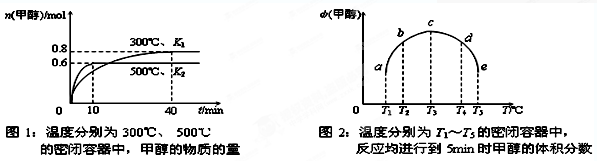
| D.图4表示在容积相同的恒容密闭容器中,等量的N02在不同温度下反应: |
 N204(g),相同时间后测得N02含量的曲线,则该反应的△H<O
N204(g),相同时间后测得N02含量的曲线,则该反应的△H<OD
A不正确,应该是面心立方堆积;钢闸门应与电源的正极相连,则作阳极失去电子,加快腐蚀,B不正确,应该是和电源的负极相连;随着醋酸的稀释,溶液的酸性是降低的,即pH是增大的,所以选项C不正确;D中根据图像可知,当NO2的含量最小时,反应达到平衡状态,但继续升高温度,NO2的含量增加,说明升高温度平衡向逆反应方向移动,所以正反应是放热反应,D正确,答案选D。
不定项选择题:本题包括5小题,每小题4分,共计20分。每小题只有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题得O分;若正确答案包括两个选项时,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就得0分。
不定项选择题:本题包括5小题,每小题4分,共计20分。每小题只有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题得O分;若正确答案包括两个选项时,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就得0分。

练习册系列答案
相关题目
 2C(g)达平衡后,恒温,增压,平衡正向移动,平衡常数K值增大
2C(g)达平衡后,恒温,增压,平衡正向移动,平衡常数K值增大 CH3OH(g) ⊿H
CH3OH(g) ⊿H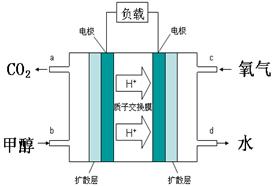
 CO(g)+H2(g);ΔH= 。(用含ΔH1、ΔH2的代数式表示)
CO(g)+H2(g);ΔH= 。(用含ΔH1、ΔH2的代数式表示)