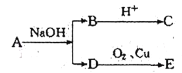
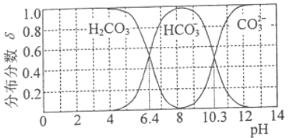
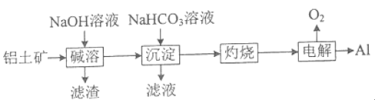
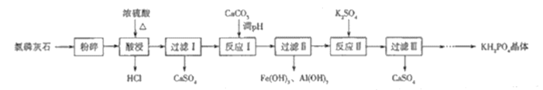
题目内容
【题目】以铅蓄电池为电源.将CO2转化为乙烯的装置如图所示,电解所用电极材料均为惰性电极。下列说法不正确的是( )
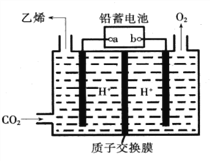
A. b为铅蓄电池的正极
B. 每生成1mol乙烯,理论上铅蓄电池中消耗12mol硫酸
C. 电解过程中,阳极区溶液中c(H+)逐渐减小
D. 阴极反应式:2CO2+12H++12e-=C2H4+4H2O
【答案】C
【解析】A、右边通入二氧化碳在电极上得电子产生乙烯,则电极为阴极,连接的电极a为负极,故b为正极,选项A正确;B、根据电极反应式:2CO2+12e-+12H+=C2H4+4H2O,每生成1mol乙烯,转移电子12mol,铅蓄电池工作的电极总反应为:Pb+PbO2+2H2SO4=2PbSO4+2H2O,每转移12mol电子,消耗12mol硫酸,选项B正确;C、电解过程中,阳极电极反应式为:2H2O-4e-=4H++O2↑,阳极区溶液中c(H+)逐渐增大,选项C不正确;D、阴极反应式:2CO2+12H++12e-=C2H4+4H2O,选项D正确。答案选C。

 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案【题目】下表是元素周期表的一部分,针对表中的①~⑩种元素,请用化学用语回答下列问题:
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ⑥ | ⑦ | ⑧ | |||||
3 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
4 | ② | ④ |
(1)在③~⑦元素中,原子半径最大的是__________(填元素符号);
(2)⑦元素的最高价氧化物对应的水化物与其氢化物能生成盐M,M中含有的化学键类型有__________________;
(3)写出元素①和⑧的单质在加热条件下反应生成的化合物的电子式:_________。
(4
(5)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是_____________(填物质化学式);呈两性的氢氧化物是_________(填物质化学式),该化合物与NaOH溶液反应的离子方程式为___________。
(6)用电子式表示元素③与⑨形成化合物的过程_____________________________。