题目内容
13.A元素的L层比B元素的L层少3个电子,B元素原子的核外电子总数比A元素多5个,由此可推知,A是N,B是Mg.分析 A元素原子的L层比B元素原子的L层少3个电子,则A的L层电子应为5,原子核外电子数为7,B元素原子核外电子数比A元素原子核外电子总数多5个,则B的原子核外电子数应为12,以此解答该题.
解答 解:A、B两元素原子的L层上有电子,则K层上肯定填满2个,而B原子核外电子总数比A原子核外电子总数多5,
所以A元素的原子的结构示意图为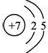 ,B元素原子核外电子数比A元素原子核外电子总数多5个,则B的原子核外电子数应为12,B元素原子的结构的示意图为
,B元素原子核外电子数比A元素原子核外电子总数多5个,则B的原子核外电子数应为12,B元素原子的结构的示意图为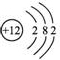 ,即A为N元素,B为Mg元素,
,即A为N元素,B为Mg元素,
故答案为:N;Mg.
点评 本题考查原子的结构与性质,题目难度不大,注意把握原子核外电子排布的关系.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.等体积、等浓度的浓硫酸分别与足量的炭粉、铜粉在一定条件下完全反应.下列指定“物理量”之比不是2:1的是( )
| A. | 转移电子的物质的量 | B. | 产生SO2的物质的量 | ||
| C. | 氧化剂的物质的量 | D. | 生成水的物质的量 |
1.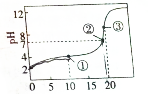 25℃时,向20mL0.2mo•lL-1HR溶液中逐渐滴入0.2mol•L-1NaOH溶液,得到如图的滴定曲线.下列粒子浓度的关系式错误的是( )
25℃时,向20mL0.2mo•lL-1HR溶液中逐渐滴入0.2mol•L-1NaOH溶液,得到如图的滴定曲线.下列粒子浓度的关系式错误的是( )
 25℃时,向20mL0.2mo•lL-1HR溶液中逐渐滴入0.2mol•L-1NaOH溶液,得到如图的滴定曲线.下列粒子浓度的关系式错误的是( )
25℃时,向20mL0.2mo•lL-1HR溶液中逐渐滴入0.2mol•L-1NaOH溶液,得到如图的滴定曲线.下列粒子浓度的关系式错误的是( )| A. | 点①溶液中,c(HR)+2c(H+)=c(R-)+2c(OH-) | |
| B. | 点②溶液中,c(Na+)=c(HR)+c(R-) | |
| C. | 点③溶液中,c(Na+)>c(R-)>(OH-)>c(H+) | |
| D. | 滴定过程中可能会出现,c(HR)>c(R-)>(H+)>c(Na+) |
 和
和