题目内容
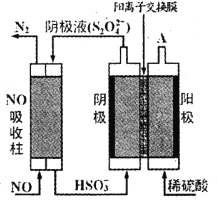
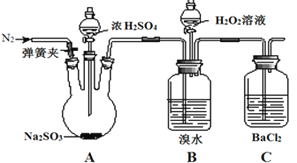
【题目】为探究H2O2、SO2、Br2的性质,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验)。
实验操作 | 实验现象 |
i.打开弹簧夹,通入N2一段时间,关闭弹簧夹,打开A中分液漏斗活塞,滴加浓硫酸 | A中有气泡产生,B中红棕色溴水褪色,C中有白色沉淀 |
ⅱ.取C中沉淀加入盐酸 | C中白色沉淀不溶解 |
ⅲ.打开B中分液漏斗活塞,逐滴滴加H2O2 | 开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色 |
(1)在滴入浓硫酸之前要通入N2一段时间的目的是__________________________。
(2)该实验可以证明SO2具有_________性;H2O2的氧化性_________Br2(填“强于”“弱于”)。
(3)B中红棕色褪去的原因_______________________________,B中重新变成红棕色的原因____________________________________(均用离子方程式表示)。
(4)C中产生的白色沉淀是______。
(5)甲同学通过C中产生白色沉淀,得出结论:SO2能与BaCl2反应产生沉淀。乙同学认为不能得出此结论,并对实验进行了改进:在B和C之间增加盛放_________的洗气瓶。再次进行实验时,则C中未产生沉淀。
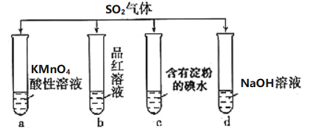
(6)为进一步研究SO2的性质,分别用煮沸和未煮沸过的蒸馏水配制Ba(NO3)2和BaCl2溶液,进行如下实验:
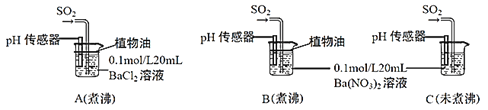
①实验A中,没有观察到白色沉淀,但pH传感器显示溶液呈酸性,原因是__________________。(用化学方程式表示)
②实验C中出现白色沉淀比实验B快很多。由此得出的结论是__________________。若实验B、C中通入足量的SO2后,溶液酸性:B_________C(填“强于”“弱于”“等于”)。
(7)Na2SO3固体因贮放不慎发生变质。现取样品1.8克溶于水得溶液A,在A中加入足量BaCl2溶液,过滤得沉淀B,将沉淀B加入足量的稀硫酸后,沉淀不仅不消失,反而增加了0.16g(假如沉淀完全转化)。样品中Na2SO3的质量分数是___________________。
【答案】排净装置内空气 还原性 强于 SO2+Br2+2H2O=SO42-+2Br-+4H+ 2Br-+H2O2+2H+=Br2+2H2O BaSO4 CCl4 SO2+H2OH2SO3 在水溶液中O2氧化SO2的速率比NO3﹣快 弱于 70%
【解析】
(1)装置中含有空气,空气中的氧气能和SO2在水溶液中发生氧化还原反应生成H2SO4,在滴加浓硫酸之前应增加一步操作,先排尽空气,则滴入浓硫酸之前要通入N2一段时间的目的是排净装置内空气;
(2)SO2使溴水褪色,体现了SO2具有还原性;实验ⅲ中在含有Br-的水溶液中滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色,说明Br-被氧化为Br2,则由氧化剂的氧化性大于氧化产物可知,H2O2的氧化性大于Br2;
(3)B中红棕色褪去是Br2被SO2还原为Br-,发生的离子反应方程式为SO2+Br2+2H2O=SO42-+2Br-+4H+;在含有Br-的水溶液中滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色,说明Br-被氧化为Br2,发生的离子反应方程式为2Br-+H2O2+2H+=Br2+2H2O;
(4)C中产生的白色沉淀不溶于稀盐酸,则此沉淀应为BaSO4;
(5)由于溴单质有挥发性,溴单质在水溶液可以将SO2氧化成H2SO4,再与BaCl2溶液反应生成BaSO4沉淀,则应该在B和C之间增加洗气瓶D来除去挥发的溴蒸气,D中盛放的试剂是CCl4或苯或饱和NaHSO3溶液;
(6)①二氧化硫与水反应生成亚硫酸,亚硫酸溶液呈酸性,涉及反应为SO2+H2OH2SO3,生成的亚硫酸再发生电离:H2SO3H++HSO3-;
②实验C中出现白色沉淀比实验B快很多C中未煮沸,则有氧气参与反应,速率较快,则说明在水溶液中O2氧化SO2的速率比NO3﹣快,C生成更多的硫酸,溶液的酸性强,即B中酸性弱于C中;
(7)部分氧化的Na2SO3固体溶于水得溶液A中加入足量BaCl2溶液,生成的沉淀B为BaSO4和BaSO3的混合物,再加入足量的稀硫酸后,沉淀不仅不消失,反而增加了0.16g,说明全部转化为BaSO4沉淀;已知1molBaSO3完全转化为1molBaSO4,质量增重233g-217g=16g,则沉淀增加0.16g,说明参加反应的BaSO3为![]() =0.01mol,则样品中Na2SO3的质量分数是
=0.01mol,则样品中Na2SO3的质量分数是![]() ×100%=70%。
×100%=70%。