题目内容
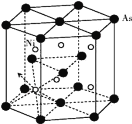
【题目】下图有机物的正确命名为 ( )

A.2-乙基-3,3-二甲基戊烷B.3,3-二甲基-4-乙基戊烷
C.3,3,4-三甲基己烷D.3,4,4-三甲基己烷
【答案】C
【解析】
烷烃命名时,要选最长的碳链为主链,据此得出是“某烷”,然后从离支链近的一端给主链上的碳原子进行编号,当两端离支链一样近时,要从支链多的一端开始编号,将取代基写在“某烷”的前面,据此分析。
烷烃命名时,要选最长的碳链为主链,此烷烃的主链有6个碳原子,故为己烷,从离支链近的一端给主链上的碳原子进行编号,而当两端离支链一样近时,要从支链多的一端开始编号,故在3号碳原子上有两个甲基,在4号碳原子上有一个甲基,则该有机物的名称为3,3,4三甲基己烷,故C正确;
答案选C。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目