题目内容
【题目】某酸式盐NaHY的水溶液c(OH-)>c(H+),下列叙述正确的是
A. H2Y的电离方程式:H2Y![]() 2H++Y2-
2H++Y2-
B. HY-的水解方程式:HY-+ H2O![]() H3O++ Y2-
H3O++ Y2-
C. 该酸式盐溶液中离子浓度关系:c(Na+)>c(HY-)>c(OH-)>c(H+)
D. 该酸式盐溶液中离子浓度关系:c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+)
【答案】C
【解析】
试题A、H2Y是二元弱酸,电离时分两步电离,第一步电离生成氢离子和酸式酸根离子,电离方程式为:H2Y+H2OHY-+H3O+,故A错误;B、HY-离子水解生成H2Y,所以HY-离子水解的离子方程式:HY-+H2OH2Y+OH-,故B错误;C、D某酸的酸式盐NaHY的水溶液中,阴离子水解,钠离子不水解,所以c(Na+)>c(HY-);HY-的电离程度小于HY-的水解程度,所以c(H2Y)>c(H+)>c(Y2-),但无论电离还是水解都较弱,阴离子还是以HY-为主,溶液呈碱性,说明溶液中c(OH-)>c(H+);因溶液中还存在水的电离,则c(H+)>c(Y2-),所以离子浓度大小顺序为c(Na+)>c(HY-)>c(OH-)>c(H2Y)>c(H+)>c(Y2-),故C正确;D错误;

【题目】由A、B、C、D四种金属按下表中装置进行实验。
装置 |
|
|
|
现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是______________________________________。
(2)装置乙中正极的电极反应式是_______________________________________。
(3)装置丙中溶液的pH________(填“变大”、“变小”或“不变”)。
(4)四种金属活动性由强到弱的顺序是___________________________________。
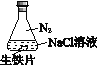
【题目】研究生铁的锈蚀,下列分析不正确的是
序号 | ① | ② | ③ |
实验 |
|
|
|
现象 | 8小时未观察 到明显锈蚀 | 8小时未观察 到明显锈蚀 | 1小时观察 到明显锈蚀 |
A. ①中,NaCl溶液中溶解的O2不足以使生铁片明显锈蚀
B. ②中,生铁片未明显锈蚀的原因之一是缺少H2O
C. ③中正极反应:O2+4e+ 2H2O ==4OH
D. 对比①②③,说明苯能隔绝O2