��Ŀ����
����Ŀ��ij��ѧС�����û������Ʊ�����ϩ���������������£���Ӧԭ����  ��Ӧ���������������ʣ�
��Ӧ���������������ʣ�
�ܶȣ�g/cm3�� | �۵㣨�棩 | �е㣨�棩 | �ܽ��� | |
������ | 0.96 | 25 | 161 | ������ˮ |
����ϩ | 0.81 | ��103 | 83 | ������ˮ |
��1��ʵ������п��ܷ������л�����Ӧ�ķ���ʽΪ ��
��2�������������ϣ�װ�ã�A��B��C��������������ɱ����Ʊ�ʵ�飮 
��3���Ʊ��ֲ�Ʒ ��5mL�����Թ�A�У��ټ���10m �� ҡ�Ⱥ�������Ƭ��������������Ӧ��ȫ��
��4���ֲ�Ʒ�ᴿ �ٻ���ϩ�ֲ�Ʒ�к��л������������������ʵȣ��ֲ�Ʒ�����ξ���ˮϴ����̼������Һϴ���Լ��ڶ���ˮϴ���ڴ˹����м���̼������Һ��Ŀ��������Һʱ������ϩӦ�ӷ�Һ©��������ϡ����¡�����ȡ����
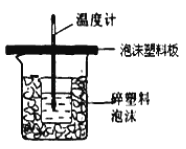
����ˮϴ��Ļ���ϩ�м�����������ˮ�Ȼ��ƣ��ٽ���������ͼD��ʾװ�õ������������ƣ��У����������ռ���Ʒʱ���¶ȼ���ʾ���¶�ӦΪ ��
���𰸡�
��1��![]()
��2��C
��3����������Ũ����
��4����ȥ����ϩ�������������ʣ��ϣ�������ƿ��85��
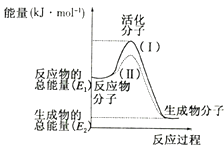
���������⣺��1����Ũ���������������������£����ܷ���ȡ����Ӧ�����ѣ����Ը������£�����������ȡ����Ӧ�����ѣ� ��Ӧ����ʽΪ![]() ��
��
���Դ��ǣ�![]() ����2����ʵ����Ҫ���¶���85�棬������Ҫˮԡ���ȣ��¶ȼ�Ӧ�ò���ˮԡ�¶ȣ�Ȼ����������ķ�����ȡ�������ѡȡ��װ��Ӧ����C����ѡC����3����Ӧװ����Ӧ���ȼ��ܶ�С�����ʺ���ܶȴ�����ʣ��������ܶ�С��Ũ���ᣬ����Ӧ���ȼӻ��������Ũ���ᣬ�ҷ�ֹҺ�彦����������ȫ�¹ʣ����Դ��ǣ���������Ũ�����4����̼���ƺ����ᷴӦ���ɿ����Ե������ƣ��Ӷ���ȥ�����Һʱ���ϲ�Һ����Ͽڵ������²�Һ����¿ڵ���������ϩ�ܶ�С��ˮ�Ҳ�����ˮ�����Ժ�ˮ������ϲ㣬���Һʱ����ϩ�ӷ�Һ©���Ͽڵ��������Դ��ǣ���ȥ����ϩ�������������ʣ��ϣ�
����2����ʵ����Ҫ���¶���85�棬������Ҫˮԡ���ȣ��¶ȼ�Ӧ�ò���ˮԡ�¶ȣ�Ȼ����������ķ�����ȡ�������ѡȡ��װ��Ӧ����C����ѡC����3����Ӧװ����Ӧ���ȼ��ܶ�С�����ʺ���ܶȴ�����ʣ��������ܶ�С��Ũ���ᣬ����Ӧ���ȼӻ��������Ũ���ᣬ�ҷ�ֹҺ�彦����������ȫ�¹ʣ����Դ��ǣ���������Ũ�����4����̼���ƺ����ᷴӦ���ɿ����Ե������ƣ��Ӷ���ȥ�����Һʱ���ϲ�Һ����Ͽڵ������²�Һ����¿ڵ���������ϩ�ܶ�С��ˮ�Ҳ�����ˮ�����Ժ�ˮ������ϲ㣬���Һʱ����ϩ�ӷ�Һ©���Ͽڵ��������Դ��ǣ���ȥ����ϩ�������������ʣ��ϣ�
�ڽ�������ʱʢ��ҩƷ��������������ƿ�����ݷ�Ӧ�¶�ֵ���ռ���Ʒ��Ҫ���¶���85�棬���Դ��ǣ�������ƿ��85�森

 ��У����ϵ�д�
��У����ϵ�д�