题目内容
【题目】在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示.请认真观察如图,然后回答问题: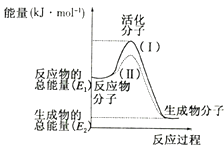
(1)图中所示反应是(填“吸热”或“放热”)反应,该反应的△H=(用含E1、E2的代数式表示).
(2)下列4个反应中符合示意图描述的反应的是 (填代号).
A.水蒸气与炭反应
B.用水稀释氢氧化钠溶液
C.铝粉与Fe2O3反应
D.灼热的碳与CO2反应
(3)已知热化学方程式:H2(g)+ ![]() O2 (g)=H2O(g)△H=﹣241.8kJ/mol.该反应的活化能为167.2kJ/mo1,则其逆反应的活化能为 .
O2 (g)=H2O(g)△H=﹣241.8kJ/mol.该反应的活化能为167.2kJ/mo1,则其逆反应的活化能为 .
(4)以甲烷为原料制取氢气是工业上常用的制氢方法.已知:
CH4 (g)+H2O(g)=CO(g)+3H2(g)△H=+206.2kJ/mol
CH4(g)+CO2(g)=2CO(g)+2H2 (g)△H=+247.4kJ/mol
CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为 .
【答案】
(1)放热,(E2﹣E1 )KJ/mol
(2)C
(3)409.0KJ/mol
(4)CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=165.0kJ/mol
【解析】解:(1)依据图象分析反应物的能量大于生成物的能量,反应放热;在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才能发生化学反应,反应需要能量;反应的焓变=生成物的能量﹣反应物的能量;△H=(E2﹣E1 )KJ/mol;故答案为:放热;(E2﹣E1 )KJ/mol;(2)图示物质反应前后能量变化礼服业务能量高于生成物反应是放热反应,
A.水蒸气与炭反应需要高温进行,反应是吸热反应,故A不符合;
B.用水稀释氢氧化钠溶液过程中溶液温度变化不大,不是化学反应,故B不符合;
C.铝粉与Fe2O3反应,引发后反应继续进行为放热反应,故C符合;
D.灼热的碳与CO2反应属于吸热反应,故D不符合;
故答案为:C;(3)反应的活化能是使普通分子变成活化分子所需提供的最低限度的能量,依据图象能量关系可知,逆反应的活化能=正反应的活化能+反应的焓变;H2(g)+ ![]() O2(g)═H2O(g)△H=﹣241.8kJmol﹣1,该反应的活化能为167.2kJmol﹣1,则其逆反应的活化能=167.2KJ/mol+241.8KJ/mol=409.0KJ/mol;
O2(g)═H2O(g)△H=﹣241.8kJmol﹣1,该反应的活化能为167.2kJmol﹣1,则其逆反应的活化能=167.2KJ/mol+241.8KJ/mol=409.0KJ/mol;
故答案为:409.0KJ/mol;(4)①CH4(g)+H2O(g)═CO(g)+3H2(g)△H=+206.2kmol﹣1②CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=+247.4kJmol﹣1
据盖斯定律,①×2﹣②得:CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=165.0kmol﹣1,故答案为:CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=+165.0kmol﹣1.
(1)依据图象分析反应物的能量大于生成物的能量,反应放热;在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才能发生化学反应,反应需要能量;反应的焓变=生成物的能量﹣反应物的能量;(2)图示物质反应前后能量变化,反应物能量高于生成物能量,反应是放热反应,据此分析选项中的反应是放热反应的符合;(3)反应的活化能是使普通分子变成活化分子所需提供的最低限度的能量,依据图象能量关系可知,逆反应的活化能=正反应的活化能+反应的焓变;(4)从待求反应出发分析反应物、生成物在所给反应中的位置,通过相互加减可得,据盖斯定律,①×2﹣②得到.

【题目】某化学小组准备用环己醇制备环己烯,查得相关资料如下.反应原理:  反应物与产物的物理性质:
反应物与产物的物理性质:
密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
环己醇 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 0.81 | ﹣103 | 83 | 难溶于水 |
(1)实验过程中可能发生的有机副反应的方程式为 .
(2)根据上述资料,装置(A,B,C)最适宜用来完成本次制备实验. 
(3)制备粗产品 将5mL加入试管A中,再加入10m , 摇匀后放入碎瓷片,缓慢加热至反应完全.
(4)粗产品提纯 ①环己烯粗产品中含有环己醇和少量酸性杂质等.粗产品需依次经过水洗、加碳酸钠溶液洗涤以及第二次水洗.在此过程中加入碳酸钠溶液的目的是;分液时,环己烯应从分液漏斗的(填“上”或“下”)口取出.
②向水洗后的环己烯中加入少量的无水氯化钙,再将混合物放入图D所示装置的(填仪器名称)中,进行蒸馏,收集产品时,温度计显示的温度应为 .