题目内容
【题目】实验室制备硝基苯的实验装置如图所示(夹持装置已略去)。下列说法错误的是( )
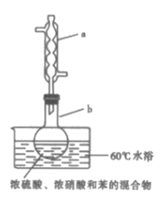
A.水浴加热的优点为使反应物受热均匀、容易控制温度
B.浓硫酸、浓硝酸和苯混合时,应先向浓硝酸中缓缓加入浓硫酸,待冷却至室温后,再将苯逐滴滴入
C.仪器a的作用是冷凝回流,提高原料的利用率
D.可用仪器a、b将反应后的混合物直接蒸馏得到产品
【答案】D
【解析】
A.水浴加热的优点是使反应物受热均匀、容易控制温度,A正确;
B.混合时先加浓硝酸,后加浓硫酸,待混合液冷却至室温后,再加入苯,B正确;
C.冷凝管可冷凝回流反应物,则仪器a的作用是冷凝回流,提高原料的利用率,C正确;
D.反应完全后,由于硝基苯是密度比水大,难溶于水的液体物质,而酸溶解在水中,因此硝基苯与酸分层,硝基苯在下层,酸溶液在上层,应先分液分离出有机物,再蒸馏分离出硝基苯,D错误;
故合理选项是D。

【题目】依据事实,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为___。
(2)25℃、101kPa若适量的N2和O2完全反应,每生成23gNO2需要吸收16.95kJ热量___。
(3)25℃、101kPa已知拆开1mol H-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为___。
(4)甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)![]() CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
③CO2(g)+H2(g)![]() CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3
回答下列问题:
已知反应①中相关的化学键键能数据如下:
化学键 | H—H | C—O | C | H—O | C—H |
E/(kJ·mol-1) | 436 | 343 | 1076 | 465 | 413 |
由此计算△H1=___kJ·mol-1,已知△H2=-58kJ·mol-1,则△H3=___kJ·mol-1。