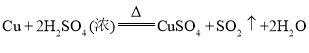题目内容
【题目】铬、钼![]() 、钨
、钨![]() 都是ⅥB族元素,且原子序数依次增大,它们的单质和化合物在生活、生产中有广泛应用。
都是ⅥB族元素,且原子序数依次增大,它们的单质和化合物在生活、生产中有广泛应用。
![]() 铬元素的最高化合价为________;基态钼原子的核外电子排布类似于基态铬原子,其原子核外有________个未成对电子。
铬元素的最高化合价为________;基态钼原子的核外电子排布类似于基态铬原子,其原子核外有________个未成对电子。
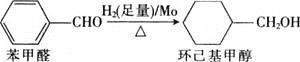
![]() 钼可作有机合成的催化剂。例如,苯甲醛被还原成环己基甲醇。
钼可作有机合成的催化剂。例如,苯甲醛被还原成环己基甲醇。
![]() 环己基甲醇分子中采取
环己基甲醇分子中采取![]() 杂化的原子是________
杂化的原子是________![]() 写元素符号
写元素符号![]() 。
。
![]() 环己基甲醇的沸点高于苯甲醛,其原因是________。
环己基甲醇的沸点高于苯甲醛,其原因是________。
![]() 铬离子
铬离子![]() 能形成多种配合物,例如
能形成多种配合物,例如![]() 。
。
![]() 已知配合物的中心粒子的配位数指配位原子总数。上述配合物中,
已知配合物的中心粒子的配位数指配位原子总数。上述配合物中,![]() 的配位数为________。
的配位数为________。
![]() 上述配合物中的非金属元素按电负性由小到大的顺序排列为________。
上述配合物中的非金属元素按电负性由小到大的顺序排列为________。
![]() 铬的一种氧化物的晶胞结构如图所示。
铬的一种氧化物的晶胞结构如图所示。
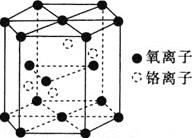
![]() 该氧化物的化学式为________。
该氧化物的化学式为________。
![]() 已知晶胞底面的边长为acm,晶胞的高为bcm,
已知晶胞底面的边长为acm,晶胞的高为bcm,![]() 代表阿伏加德罗常数的值,该铬的氧化物的摩尔质量为
代表阿伏加德罗常数的值,该铬的氧化物的摩尔质量为![]() 。该晶体的密度为________
。该晶体的密度为________![]() 用含a、b、
用含a、b、![]() 和M的代数式表示
和M的代数式表示![]() 。
。
【答案】![]() 6
6 ![]() 、O 环己基甲醇分子间能够形成氢键
、O 环己基甲醇分子间能够形成氢键 ![]()
![]()
![]()
![]()
【解析】
(1)Cr位于周期表中第4周期第ⅥB族,最高化合价为+6,基态钼原子的核外电子排布类似于基态铬原子,根据Cr的电子排布解答;
(2)①环己基甲醇分子中,C和O均满足八隅体,C和O均达到饱和;
②环己基甲醇的分子间存在氢键;
(3)①配合物的中心粒子的配位数指配位原子总数,OH-和H2O均为单齿配体,H2NCH2CH2NH2为双齿配体;
②上述配合物中,非金属元素有C、H、O、N,同周期主族元素,随着原子序数增大,电负性增大;
(4)①每个晶胞中含有![]() 数目为:4;
数目为:4;![]() 数目为:
数目为:![]() ;
;
![]() 每个晶胞的质量
每个晶胞的质量![]() ,晶胞的体积
,晶胞的体积![]() ,再结合
,再结合![]() 计算即可。
计算即可。
![]() 为24号元素,价电子排布式为
为24号元素,价电子排布式为![]() ,最高正价为
,最高正价为![]() 价;基态钼原子的核外电子排布类似于基态铬原子,价电子排布式为
价;基态钼原子的核外电子排布类似于基态铬原子,价电子排布式为![]() ,其原子核外有6个未成对电子;
,其原子核外有6个未成对电子;
![]() 环己基甲醇中C均以单键连接,采取
环己基甲醇中C均以单键连接,采取![]() 杂化,O原子的杂化轨道数为4,也采取
杂化,O原子的杂化轨道数为4,也采取![]() 杂化;
杂化;
![]() 环己基甲醇中含有羟基,分子间存在氢键,沸点较高;
环己基甲醇中含有羟基,分子间存在氢键,沸点较高;
![]() 中2个N原子均与
中2个N原子均与![]() 形成配位键,配体有3个
形成配位键,配体有3个![]() 、1个
、1个![]() 和1个
和1个![]() ,故C
,故C![]() 的配位数为6;
的配位数为6;
![]() 同周期从左到右,元素的电负性逐渐增大,氢的电负性在四种元素中最小,故电负性:
同周期从左到右,元素的电负性逐渐增大,氢的电负性在四种元素中最小,故电负性:![]() ;
;
![]() 每个晶胞中含有
每个晶胞中含有![]() 数目为:4;
数目为:4;![]() 数目为:
数目为:![]() ,故化学式为
,故化学式为![]() ;
;
![]() 每个晶胞的质量
每个晶胞的质量![]() ,晶胞的体积
,晶胞的体积![]() ,故晶胞的密度
,故晶胞的密度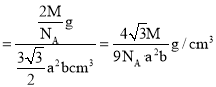 。
。

【题目】(某化学兴趣小组制取氯酸钾和氯水并进行有关探究实验。
实验一 制取氯酸钾和氯水
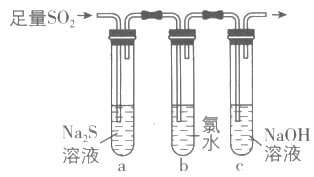
利用下图所示的实验装置进行实验。
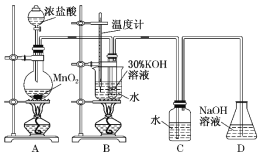
(1)制取实验结束后,取出B中试管冷却结晶,过滤,洗涤。该实验操作过程需要的玻璃仪器有________。
(2)若对调B和C装置的位置,________(填“能”或“不能”)提高B中氯酸钾的产率。
实验二 氯酸钾与碘化钾反应的研究
(3)在不同条件下KClO3可将KI氧化为I2或KIO3。该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如下(实验在室温下进行):
试管编号 | 1 | 2 | 3 | 4 |
0.20 mol·L-1 KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
6.0 mol·L-1H2SO4/mL | 0 | 3.0 | 6.0 | 9.0 |
蒸馏水/mL | 9.0 | 6.0 | 3.0 | 0 |
实验现象 |
①系列a实验的实验目的是________________。
②设计1号试管实验的作用是________________。
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为___________________________。
实验三 测定饱和氯水中氯元素的总量
(4)该小组设计的实验方案为使用下图装置,加热15.0 mL饱和氯水试样,测定产生气体的体积。此方案不可行的主要原因是__________________________。(不考虑实验装置及操作失误导致不可行的原因)
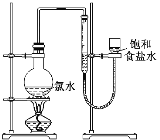
(5)根据下列资料,为该小组设计一个可行的实验方案(不必描述操作过程的细节):______________________________________________________________________。
资料:ⅰ.次氯酸会破坏酸碱指示剂;
ⅱ.次氯酸或氯气可被SO2、H2O2和FeCl2等物质还原成Cl-。