题目内容
【题目】铂钴合金是以铂为基含钴二元合金,在高温下,铂与钻可无限互溶,其固体为面心立方晶格。铂钻合金磁性极强,磁稳定性较高,耐化学腐蚀性很好,主要用于航天航空仪表、电子钟表、磁控管等。氟及其化合物CuF用途非常广泛。回答下列问题:
(1)聚四氟乙烯是一种准晶体,准晶体是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过________________方法区分晶体、准晶体和非晶体。
(2)基态F原子的价层电子排布图(轨道表达式)为________________。
(3) [H2F]+[SbF6]ˉ (氟锑酸)是一种超强酸,存在[H2F]+,该离子的空间构型为______________,与[H2F]+具有相同空间构型且中心原子与F原子同周期的分子是_____________。
(4)NH4F(氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。![]() 中心原子的杂化类型是____________;氟化铵中存在_______________(填字母)。
中心原子的杂化类型是____________;氟化铵中存在_______________(填字母)。
A.离子键 B.σ键 C.π键 D.氢键
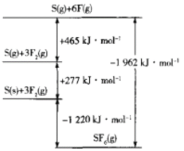
(5)SF4被广泛用作高压电气设备的绝缘介质。SF4是一种共价化合物,可通过类似于Bom-Haber循环能量构建能量图计算相关键能。则F-F键的键能为_____kJ/mol,S-F键的键能为______ kJ/mol。
(6)CuCl的熔点为326℃,能升华,熔化呈液态时不导电;CuF的熔点为1008℃,熔化呈液态时能导电。
①CuF中Cu+的基态价电子排布式________铜元素位于元素周期________区,金属Cu的堆积模型为__________________。
②CuF的熔点比CuCl的高,原因是______________
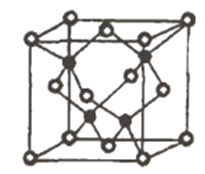
③已知NA为阿伏加德罗常数的值,CuF的密度为7.1g/cm3,晶胞结构如图所示,则CuF的晶胞参数a=_______nm(列出计算式)
【答案】X-射线衍射实验 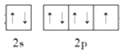 V形 H2O sp3 AB 155 327 3d10 ds 面心立方最密堆积 CuF为离子晶体,CuCl为分子晶体
V形 H2O sp3 AB 155 327 3d10 ds 面心立方最密堆积 CuF为离子晶体,CuCl为分子晶体 ![]() ×107
×107
【解析】
(2)根据核外电子排布规律写出F的核外电子排布,再画出价电子排布图;
(3)根据同族替换和等量代换原则找等电子体,等电子体具有相同的空间构型;
(4)根据价层电子对互斥理论判断原子的杂化方式;
(5)在标准状况下,将1mol气态分子解离为气态原子所需的能量;
(6)离子晶体熔沸点高于分子晶体;根据均摊法计算晶胞中各微粒的数目,确定晶胞的质量,根据![]() 计算晶胞参数。
计算晶胞参数。
(1)从外观无法区分晶体、准晶体和非晶体,但用X光照射会发现:晶体对X射线发生衍射,非晶体不发生衍射,准晶体介于二者之间,因此通过X-射线衍射实验可区分晶体、准晶体和非晶体;
(2)F的原子序数为9,核外电子排布式为1s22s22p5,价电子为2s22p5,因此基态F原子的价电子排布图为 ;
;
(3)[H2F]+的中心原子的价层电子对数为![]() =4,含有两对孤对电子,所以空间构型为V形;原子总数相同,价电子总数相同的分子或离子互为等电子体,结构相似,所以与[H2F]+具有相同空间构型且中心原子与F原子同周期的分子是H2O;
=4,含有两对孤对电子,所以空间构型为V形;原子总数相同,价电子总数相同的分子或离子互为等电子体,结构相似,所以与[H2F]+具有相同空间构型且中心原子与F原子同周期的分子是H2O;
(4)![]() 中心原子的价层电子对数为4,所以为sp3杂化;NH4F中氟离子和铵根之间为离子键,铵根内部共价键和配位键均为σ键,所以选AB;
中心原子的价层电子对数为4,所以为sp3杂化;NH4F中氟离子和铵根之间为离子键,铵根内部共价键和配位键均为σ键,所以选AB;
(5)由图象可知,3molF2(g)形成F(g)断裂3molF-F键,吸收465kJ能量,则F-F键的键能为155kJmol-1;由图可知1molS(g)和6molF(g)形成SF6(g)要形成6molS-F键,放出1962kJ能量,则S-F的键能为![]() kJmol-1=327kJmol-1;
kJmol-1=327kJmol-1;
(6)①Cu元素为29号元素,基态Cu原子的核外电子排布式为1s22s22p63s23p63d104s1,失去最外层一个电子形成Cu+,所以Cu+的价电子排布式为3d10;铜元素位于第四周期第IB族,所以属于ds区;金属铜为面心立方最密堆积;
②CuCl的熔点为426℃,熔化时几乎不导电,应为分子晶体,而CuF为离子晶体,一般离子晶体的熔沸点比分子晶体高,所以CuF比CuCl熔点高;
③根据均摊法,晶胞内部黑球个数为4,晶体化学式为CuF,所以白球个数也为4,即晶胞中有4个亚铜离子和4个氟离子,所以晶胞的质量为m=![]() g,晶胞体积V=a3,晶体的密度
g,晶胞体积V=a3,晶体的密度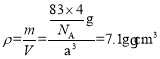 ,可解得a=
,可解得a=![]() ×107nm。
×107nm。

 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案【题目】某小组探究Na2S溶液与KMnO4溶液反应,实验过程如下:
实验序号 | Ⅰ | Ⅱ |
实验过程 | 滴加6滴(约0.3mL)0.01mol/LNa2S溶液
| 滴加6滴(约0.3mL)0.01mol/L酸性KMnO4溶液(H2SO4酸化至pH=0)
|
实验现象 | 紫色变浅(pH<1),生成棕褐色沉淀(MnO2) | 溶液呈淡黄色(pH≈8),生成浅粉色沉淀(MnS) |
资料:ⅰ.![]() 在强酸性条件下被还原为Mn2+,在近中性条件下被还原为MnO2。
在强酸性条件下被还原为Mn2+,在近中性条件下被还原为MnO2。
ⅱ.单质硫可溶于硫化钠溶液,溶液呈淡黄色。
下列说法不正确的是( )。
A.根据实验可知,Na2S被氧化
B.取少量实验Ⅰ所得溶液进行实验,检测到有![]() ,不能说明S2-被
,不能说明S2-被![]() 氧化为
氧化为![]()
C.实验Ⅰ中生成棕褐色沉淀,说明酸性条件下S2-能将![]() 还原为MnO2
还原为MnO2
D.实验Ⅱ得到浅粉色沉淀,是由于S2-将新生成的![]() 还原为Mn2+并迅速与其结合所致
还原为Mn2+并迅速与其结合所致
【题目】氮可形成多种氧化物,如NO、NO2、N2O4等。已知NO2和N2O4的结构式分别是![]() 和
和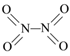 。实验测得N-N键键能167kJ·mol-1,NO2中氮氧键的平均键能466 kJ·mol-1,N2O4中氮氧键的平均键能为438.5 kJ·mol-1。
。实验测得N-N键键能167kJ·mol-1,NO2中氮氧键的平均键能466 kJ·mol-1,N2O4中氮氧键的平均键能为438.5 kJ·mol-1。
(1)写出N2O4转化为NO2的热化学方程式_________________________
(2)对反应N2O4(g)![]() 2NO2(g),在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是______
2NO2(g),在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是______
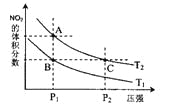
A.A、C两点的反应速率:A>C
B.B、C两点的气体的平均相对分子质量:B<C
C.A、C两点气体的颜色:A深,C浅
D.由状态B到状态A,可以用加热的方法
(3)在100℃时,将0.400mol的NO2气体充入2 L抽空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
时间(s) | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
①在上述条件下,从反应开始直至20 s时,二氧化氮的平均反应速率为_____mol·(L·s)-1。
②n3____n4(填“>”、“<”或“=”),该反应的平衡常数K的值为_____________,升高温度后,反应2NO2![]() N2O4的平衡常数K将_______(填“增大”、“减小”或“不变”)。
N2O4的平衡常数K将_______(填“增大”、“减小”或“不变”)。
③若在相同情况下最初向该容器充入的是N2
④计算③中条件下达到平衡后混合气体的平均相对分子质量为____________。(结果保留小数点后一位)